
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑩ | ⑥ | |||||
| 3 | ① | ③ | ④ | ⑧ | ⑨ | ⑦ | ||
| 4 | ② |
分析 根据元素周期表前四周期各元素的具体位置得出①到⑩的具体元素为:①Na②K③Mg④Al⑤C⑥O⑦Cl⑧Si⑨S⑩N,
(1)①③④⑨的元素符号:①Na③Mg④Al⑨S;
(2)氯元素的单质为Cl2,②为K元素灼烧火焰颜色透过蓝色古玻璃为紫色;
(3)钠与水的反应为2Na+2H2O=2NaOH+H2↑;
(4)元素⑥为氧,质子数为8,其原子核外有2个电子层.最外层电子数为6个电子;
(5)元素④为铝与⑥(氧)形成化合物的化学式为Al2O3,该化合物与盐酸反应的离子方程式为Al2O3+6H+=2Al3++3H2O;
(6)单质⑦为氯气,与石灰乳Ca(OH)2 反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的有效成分为Ca(ClO)2;
(7)元素⑩为N,它的气态氢化物的化学式为NH3,其水溶液为氨水,呈碱性;实验室用2NH4Cl与Ca(OH)2制备氨气.
解答 解:(1)①③④⑨的元素符号:①Na③Mg④Al⑨S,
故答案为:Na Mg Al S;
(2)氯元素的单质为Cl2,②为K元素灼烧火焰颜色透过蓝色古玻璃为紫色,
故答案为:Cl2 紫;
(3)钠与水的反应为2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
(4)元素⑥为氧,质子数为8,其原子核外有2个电子层.最外层电子数为6个电子,
故答案为:8 2 6;
(5)元素④为铝与⑥(氧)形成化合物的化学式为Al2O3,该化合物与盐酸反应的离子方程式为Al2O3+6H+=2Al3++3H2O,
故答案为:Al2O3+6H+=2Al3++3H2O;
(6)单质⑦为氯气,与石灰乳Ca(OH)2 反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的有效成分为Ca(ClO)2,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O; Ca(ClO)2;
(7)元素⑩为N,它的气态氢化物的化学式为NH3,其水溶液为氨水,呈碱性;实验室用2NH4Cl与Ca(OH)2制备氨气,2NH4Cl+Ca(OH)2=CaCl2+NH3↑+2H2O,
故答案为:NH3;碱;2NH4Cl+Ca(OH)2=CaCl2+NH3↑+2H2O.
点评 本题考查元素周期表与元素周期律综合应用,难度不大,注意对元素周期律的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯和水、酒精和水、苯酚和水 | |
| B. | 二溴乙烷和水、溴苯和水、硝基苯和水 | |
| C. | 甘油和水、乙醛和水、乙酸和乙醇 | |
| D. | 乙酸和水、甲苯和水、己烷和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol铜片与含2molH2SO4的浓硫酸共热 | |
| B. | 1molMnO2粉末与含2molH2O2的溶液共热 | |
| C. | 常温下1mol铝片投入足量的浓硫酸中 | |
| D. | 常温下1mol铜片投入含4molHNO3的浓硝酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2g氦气所含原子数为NA | |
| B. | 1molD2O所含电子数为12NA | |
| C. | 0.1mol单质铝与足量盐酸反应转移的电子数为0.3NA | |
| D. | 标准状况下,1L水所含分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
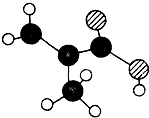 某物质只含C,H,O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等):
某物质只含C,H,O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等):
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锡靑铜的熔点比纯铜低 | |
| B. | 锡靑铜文物在潮湿环镜中的腐蚀比干燥环境中快 | |
| C. | 黄铜(铜锌合金}制作的铜锣不易产生铜绿 | |
| D. | 金属的电化学腐蚀必須在酸性条件下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 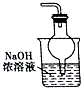 用如图装置除去乙酸乙酯中混有的少量乙酸 | |
| B. | 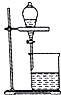 用如图装置可直接分离溴苯和溴 | |
| C. | 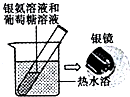 用如图装置验证葡萄糖分子有还原性 | |
| D. | 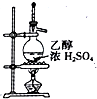 用如图装置制取乙烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com