
| A. | 乙烯通入酸性高锰酸钾溶液中 | |
| B. | 光照射甲烷与氯气的混合气体 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 苯与液溴混合后撒入铁粉 |
分析 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应;有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应,根据定义分析解答.
解答 解:A.乙烯被酸性高锰酸钾氧化使酸性高锰酸钾褪色,属于氧化反应,故A不符合;
B.甲烷和氯气在光照条件下发生取代反应,生成一氯甲烷、二氯甲烷等取代物,故B不符合;
C.在镍作催化剂的条件下,苯与氢气发生加成反应生成环己烷,故C符合;
D.苯与液溴反应,苯环上的氢原子被溴原子取代取代生成溴苯,属于取代反应,故D不符合;
故选C.
点评 本题主要考查了加成反应的判断,难度不大,注意:乙烯含有碳碳双键,所以性质较活泼,能被酸性高锰酸钾溶液氧化成二氧化碳.


科目:高中化学 来源: 题型:解答题
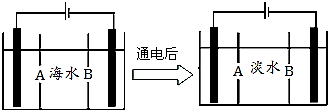 南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水.
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 失电子越多,还原性就一定越强 | |
| B. | 某元素由单质变为化合物,该元素有可能被氧化也有可能被还原 | |
| C. | 某物质焰色反应呈黄色,该物质一定含钠单质,可能含钾单质 | |
| D. | 金属氧化物一定是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
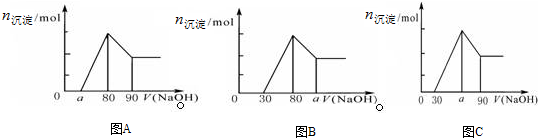
| A. | A图中a的取值范围为 0≤a<50 | |
| B. | A图中$\frac{n(Mg)}{n(Al)}$的最大值为2.5 | |
| C. | 若将关系图改为B图时,则a的取值范围为80<a<90 | |
| D. | 若将关系图改为C图时,则a的取值范围为75<a<90 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给烧瓶加热时,要垫上石棉网 | |
| B. | 给试管里的液体加热,液体体积不超过试管容积的三分之一 | |
| C. | 用托盘天平称量氢氧化钠固体时,应该放在小烧杯里称量 | |
| D. | 酒精灯打翻用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
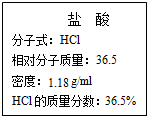 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
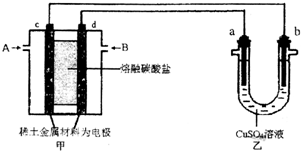
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Ca2+、NO3-、CO32- | B. | K+、H+、Fe2+、NO3- | ||
| C. | Ag+、Na+、Cl-、K+ | D. | NH4+、K+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取样品进行焰色反应,火焰显黄色,说明有Na元素存在,无K元素 | |
| B. | 向某溶液中滴入稀盐酸立即产生使澄清石灰水变浑浊的气体,说明有CO32-存在 | |
| C. | 向某溶液中滴入KSCN溶液不变色,再滴入几滴氯水变红,说明存在Fe2+,无Fe3+ | |
| D. | 向某溶液中滴加过量Ba(0H)2溶液,最终有白色沉淀,说明无Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com