
| A. | ②⑥ | B. | ②⑤ | C. | ①②⑤⑥ | D. | ②③④⑤ |
分析 ①酸指电离时所有阳离子都是氢离子的化合物;碱指电离时所有阴离子都是氢氧根离子的化合物;盐指由金属阳离子和酸根阴离子构成的化合物;两种元素组成其中一种是氧元素的化合物;
②电解质是指在水溶液中或熔融状态下能够导电的化合物,水溶液中能完全电离的电解质为强电解质,水溶液中部分电离的电解质为弱电解质;非电解质是指在水溶液中和熔融状态下能够导电的化合物;
③电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质;
④根据分散系中分散质粒子直径大小分类;
⑤有电子转移的化学反应属于氧化还原反应,根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;
⑥酸性氧化物是指和碱反应生成盐和水的氧化物,发生的反应都是复分解反应生成的盐为一种.
解答 解:①指电离时所有阳离子都是氢离子的化合物;碱指电离时所有阴离子都是氢氧根离子的化合物;盐指由金属阳离子和酸根阴离子构成的化合物;两种元素组成其中一种是氧元素的化合物;硫酸、纯碱、醋酸钠和生石灰中纯碱是盐,故①错误;
②电解质是指在水溶液中或熔融状态下能够导电的化合物,水溶液中能完全电离的电解质为强电解质,水溶液中部分电离的电解质为弱电解质;非电解质是指在水溶液中和熔融状态下能够导电的化合物,蔗糖为非电解质,硫酸钡是强电解质,水为弱电解质,故②正确;
③强电解质和弱电解质是以电解质在水溶液中能否完全电离进行定义,完全电离为强电解质,否则为弱电解质,故③错误;
④当分散剂是水或其它溶液时,根据分散质粒子直径大小来分类,把分散系划分为:溶液(小于1nm)、胶体(1nm~100nm)、浊液(大于100nm).所以,溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小.胶体粒子的直径大小在 1nm~100nm之间,故④错误;
⑤氧化还原反应的实质为电子的转移,则根据反应是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应,故⑤正确;
⑥SO2能和碱溶液发生反应属于酸性氧化物,NO2都和碱反应生成盐和水发生的是氧化还原反应,不是酸性氧化物,故⑥错误;
故选B.
点评 本题考查了物质分类、物质组成的应用,题目难度不大,掌握物质的组成和化学概念实质是解题的关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 硫单质是一种淡黄色易溶于水的固体 | |
| B. | SO2的漂白原理与活性炭相同 | |
| C. | 可用澄清石灰水鉴别SO2和CO2 | |
| D. | 可用铁质或铝质容器储存浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
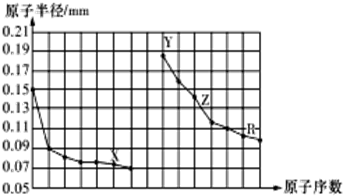
| A. | 同周期元素中,X氢化物的沸点最高 | |
| B. | 简单离子半径:X>Y>Z | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  制取并收集干燥纯净的NH3 | |
| B. |  用装置丁分离乙酸乙酯和饱和碳酸钠溶液 | |
| C. |  用于制备并收集少量NO2 | |
| D. |  比较MnO2、Cl2、S的氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com