
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| 资*源%库Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
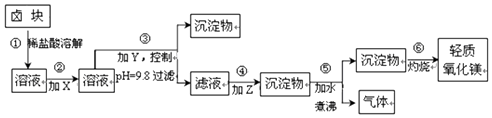
分析 为除去Fe2+,先将Fe2+氧化成Fe3+,然后加入NaOH调节pH为9.8,然后在滤液中加入纯碱将Mg2+从溶液中以MgCO3沉淀出来,然后加热煮沸可得到Mg(OH)2,灼烧后得到MgO,
(1)依据图表数据和经济效益分析加入的试剂的最佳选择;
(2)次氯酸钠具有氧化性在酸溶液中氧化亚铁离子为铁离子,据此写出反应的离子方程式;Z为碳酸钠,则步骤④生成沉淀为碳酸镁,碳酸镁在加热条件下水解生成氢氧化镁和二氧化碳气体;
(3)步骤③的目的在于使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便通过过滤而除去;
(4)步骤⑥为灼烧氢氧化镁制取氧化镁,应在坩埚中进行.
解答 解:(1)步骤②是为了将Fe2+氧化成Fe3+,并在控制合适的pH条件时生成Fe(OH)3沉淀而除之,虽然漂液和H2O2都可采用,但对比表2提供的原料价格可以看出,漂液比H2O2的价格低得多,所以选漂液最合理,故X为漂液;加入Y的目的是调节pH,选用氢氧化钠,故Y为烧碱;加入Z的目的是使镁离子沉淀,Z为纯碱;
故答案为:acd;
(2)程中加入次氯酸钠在酸性溶液中会氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++ClO-+2H+=2Fe3++Cl-+H2O;
加入的Z物质为纯碱,所以步骤④生成的沉淀物是MgCO3,所以沉淀物MgCO3在煮沸的情况下发生水解,生成Mg(OH)2和CO2气体,反应的化学方程式为:MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑,
故答案为:2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑;
(3)步骤③的目的在于使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀,以便通过过滤而除去,应加入NaOH,如加入纯碱,不能达到较高的PH,分析表1提供的数据:除去杂质离子合理的pH范围是3.7<pH<9.8,在此范围内,如果pH过高,就会有大量的Mg2+生成Mg(OH)2而进入沉淀中,从而导致生产成本的提高;为了兼顾产品质量和生产成本,选择pH=9.8最合理,当然此时Mg2+也会部分生成Mg(OH)2沉淀,但由于卤块价格低廉,这点不可避免的损失还是可以承受的,以此保证产品的纯度,
故答案为:使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去;
(4)步骤⑥由氢氧化镁灼烧制备氧化镁,应该在耐高温的坩埚中进行,
故答案为:坩埚.
点评 本题通过以卤块为原料制取轻质氧化镁的工艺流程,考查了物质制备实验方案的设计,题目难度中等,注意掌握化学基本实验操作方法,明确物质制备实验方案设计原则,本题中合理分析制取流程、得出氧化镁的制备原理为解题的关键,试题综合性较强、涉及知识点较多,充分考查了学生的分析、理解能力及化学实验能力.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ③④⑤ | C. | ②④⑥ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应放热是因为反应物的总能量低于生成物的总能量 | |
| B. | 不需要加热就能发生的反应是放热反应 | |
| C. | 化学能是能量的一种形式,它不仅可以转化为热能,也能转化为电能 | |
| D. | 释放能量的反应在常温下一定很容易发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③②①④ | B. | ①④②③ | C. | ④①②③ | D. | ②③①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4可用于鉴别溴水和碘水 | |
| B. | 用AgNO3溶液可以鉴别KCl和KI | |
| C. | 氯水久置后酸性减弱 | |
| D. | 在饱和氯水中通入H2S气体,溶液的酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯环的碳碳键键长都相等 | |
| B. | 苯分子中有C=C,所以能使溴水反应而褪色 | |
| C. | 邻-二溴苯没有同分异构体 | |
| D. | 常温下苯是一种不溶于水且密度小于水的液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤操作中,漏斗的尖端应接触烧杯内壁 | |
| B. | 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 | |
| C. | 做钠的燃烧实验,可将金属钠放在坩埚里 | |
| D. | 向容量瓶转移液体时,导流用玻璃棒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com