


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、用物质A表示的反应速率为1.2 mol/(L?s) |
| B、2 s时物质A的转化率为30% |
| C、用物质B表示的反应速率为0.6 mol/(L?s) |
| D、2 s时物质B的浓度为0.6 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
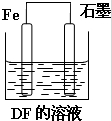 A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大.A、D同主族;A与B、C均可形成多种常见的10电子微粒;在同一周期中,简单离子半径E的最小,原子半径F的最小;B的单质分子中有三对共用电子对.请回答下列问题:
A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大.A、D同主族;A与B、C均可形成多种常见的10电子微粒;在同一周期中,简单离子半径E的最小,原子半径F的最小;B的单质分子中有三对共用电子对.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等浓度的NaCN、NaHSO3混合溶液中:c(HCN)+c(CN-)=c(HSO3-)+c(H2SO3) |
| B、pH=4.5的食醋中c(H+)是pH=6.5的番茄汁中c(H+)的100倍 |
| C、10mlpH=2的HA溶液、HB溶液分别与足量的锌反应,HA溶液放出的氢气较多,说明HA的酸性比HB的弱 |
| D、pH=4.5的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| 最高化合价 | +6 | +4 | +5 | +5 | +4 | +7 | ||
| 最低化合价 | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
| A、A的氢化物比C的氢化物稳定 |
| B、F的氢化物与H的氢化物化合所得产物为离子晶体 |
| C、F、G、H的最高价氧化物对应的水化物的酸性依次增强 |
| D、B和G的最高价氧化物均为原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| B、标准状况下,22.4 L NH3中含有共价键的数目为NA |
| C、1 molCl2与足量Fe反应转移电子数一定为3NA |
| D、标准状况下,11.2 L SO3所含的分子数目为0.5 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com