
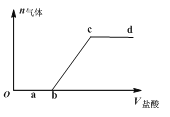
【题目】向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如下图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
A.a点对应溶液中:Ca2+、Mg2+、Br-、NO3—
B.b点对应溶液中:Al3+、Fe3+、MnO4—、NO3—
C.c点对应溶液中:Na+、Ca2+、NO3—、Cl-
D.d点对应溶液中:F-、NO3—、Fe2+、Ag+
【答案】C
【解析】
向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,由图可知,0~b发生Na2CO3+HCl=NaCl+NaHCO3,b~c发生NaHCO3+HCl=NaCl+H2O+CO2↑,c之后盐酸过量不发生反应,结合离子之间不能结合生成沉淀、气体、水等,不能相互促进水解、发生氧化还原反应等,则离子大量共存,以此来解答。
A. a点溶液中含有CO32-和HCO3-,Ca2+不能共存,故A错误;
B. b点全部为HCO3-,Al3+、Fe3+与HCO3-发生互促水解反应而不能大量共存,故B错误;
C. c点恰好完全反应生成NaCl,溶液呈中性,离子之间不发生反应,在溶液中能够大量共存,故C正确;
D. d点呈酸性,酸性条件下,NO3-与Fe2+发生氧化还原反应而不能大量共存,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、容积不变的密闭容器中进行如下反应:N2(g)+3H2(g)![]() 2NH3(g),达到平衡。下列说法不正确的是( )
2NH3(g),达到平衡。下列说法不正确的是( )
A. 其它条件不变,缩小容器体积,平衡正向移动,K值变大
B. 其它条件不变,通入少量氦气,平衡不移动
C. N2、H2、NH3百分含量不再变化
D. 其它条件不变,升高温度,化学平衡一定发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示,电极为惰性电极。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42—等离子。下列叙述中正确的是( )

A. A膜是阳离子交换膜
B. 通电后,海水中阴离子往b电极处移动
C. 通电后,b电极上产生无色气体,溶液中出现白色沉淀
D. 通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)含氢原子为0.2×6.02×1024个的NH4HCO3,其质量是___,其中含氧原子的物质的量为___。3.6克水中含有质子数为___(阿伏伽德罗常数为NA)。
(2)现实验室要用12mol·L-1氢氧化钠溶液来配制浓度为0.6mol·L-1的稀氢氧化钠溶液100mL,则需要这种浓碱的体积是___mL。需要用托盘天平称量___克氢氧化钠才能配制成0.5mol·L-1的氢氧化钠溶液100mL。
(3)将标况下aLHCl气体溶于配制成1L盐酸溶液,所得溶液密度为dg/cm3,则所得溶液物质的量浓度为___mol/L,该溶液中溶质的质量分数为___。
(4)在标准状况下,某气体A的密度是1.25g·L-1,则它的摩尔质量是___,同温同压下该气体相对于氢气的密度是___;在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,此混合气体的平均相对分子质量是___,混合物中CO和CO2物质的量之比是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚醋酸乙烯酯E是醋酸乙烯酯D的聚合物,英文缩写为PVAc,主要用作涂料,也可用作制取聚乙烯醇和聚乙烯醇缩醛的原料。工业上可用以下合成路线制取:
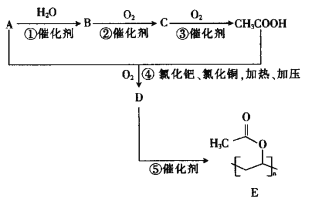
已知:A的蒸气密度相对氢气的密度是14。请回答下列问题:
(1)A的结构简式为__________,D的分子式为__________,B中官能团的名称为__________,反应⑤的反应类型为__________。
(2)完全燃烧等物质的量的A、B、C,耗氧量从大到小的顺序为__________(用字母表示)。
(3)反应④的化学方程式为________________________________________。
(4)D有多种同分异构体,既能发生水解反应,又能发生银镜反应的D的同分异构体有__________种,其中核磁共振氢谱有3组峰,且峰面积之比为1:1:4的同分异构体的结构简式为__________。
(5)根据已有知识并结合相关信息,写出以CH3CH=CH2和CH3CH2CH2OH为原料制备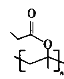 的合成路线流程图(无机试剂任用):____________________。
的合成路线流程图(无机试剂任用):____________________。
合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧杯中盛有含0.2 mol NH4Al(SO4)2的溶液,向其中缓缓加入4 mol·L-1的NaOH溶液200 mL,使其充分反应,此时烧杯中铝元素的存在形式为( )
A. Al3+和Al(OH)3 B. AlO2— C. AlO2—和Al(OH)3 D. Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去粗盐中的杂质CaCl2、MgCl2和Na2SO4,过程如下:
![]()
下列有关说法中,不正确的是( )
A. 除去Mg2+的主要反应:MgCl2+2NaOH-=Mg(OH)2↓+2NaCl
B. 试剂①一定不是Na2CO3溶液
C. 检验SO42-是否除净:取少量滤液,加稀盐酸酸化,再加BaCl2溶液
D. 滤液加稀盐酸时只发生反应:HCl+NaOH=H2O+NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H2(填“大于”或“小于”)。
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为_________(填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用![]() 标注。
标注。

可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________eV,写出该步骤的化学方程式_______________________。
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的PH2O和PCO相等、PCO2和PH2相等。
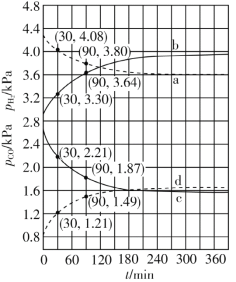
计算曲线a的反应在30~90 min内的平均速率![]() (a)=___________kPa·min1。467 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。489 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。
(a)=___________kPa·min1。467 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。489 ℃时PH2和PCO随时间变化关系的曲线分别是___________、___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com