
| 阳离子 | Ba2+ Ag+ Mg2+ Na+ |
| 阴离子 | SO42- SO32- CO32- AlO2- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
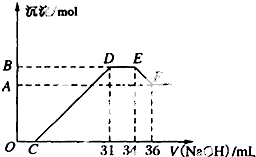 某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:
某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠的化学活泼性很强,钠着火必须及时用泡沫灭火器扑灭 |
| B、氧化钠和过氧化钠都是白色固体,都是碱性氧化物 |
| C、将金属钠投入水中,生成氢氧化钠,同时放出O2 |
| D、少量钠通常保存在煤油里 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硬水浑浊、软水澄清 |
| B、硬水含有杂质、软水含杂质少 |
| C、硬水含有较多可溶性钙镁化合物、软水不含或含少量可溶性钙镁化合物 |
| D、硬水是不纯净水,软水是纯净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) |
| B、2 c(Na+)=c(A2-)+c(HA-)+c(H2A) |
| C、c(OH-)=c(H+)+c(HA-)+c(H2A) |
| D、c(Na+)+c(H+)=2 c(A2-)+c(OH-)+c(HA-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
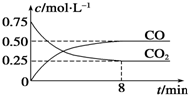 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)△H=a kJ?mol-1,测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)△H=a kJ?mol-1,测得CO2和CO浓度随时间的变化如图所示:| 温度(℃) | 500 | 700 |
| 平衡常数K | 2.00 | 2.50 |
| c(CO) |
| c(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
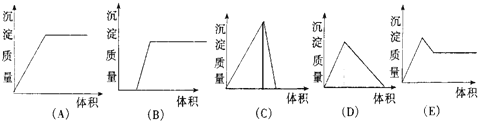
| V |
| 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com