
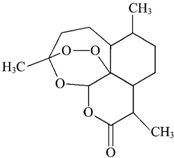
| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 该有机物属于烃 | |
| C. | 分子中含有醚键、酯基、甲基三种官能团 | |
| D. | 能发生加成反应和取代反应 |
分析 A.根据结构简式确定分子式;
B.只含C、H元素的有机物是烃;
C.该分子中含有醚键、酯基和过氧键;
D.碳不饱和键、苯环、羰基、醛基都能发生加成反应,酯基能发生取代反应.
解答 解:A.通过分析可知该有机物分子中含有15个碳原子,22个氢原子和5个氧原子,其分子式为C15H22O5,故A正确;B.该有机物中含有氧原子,不属于烃,故B错误;
C.甲基不属于官能团,该物质中还含有过氧键,故C错误;
D.该有机物含有酯基和甲基,可发生取代反应,不能发生加成反应,故D错误;
故选A.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团及其性质关系是解本题关键,侧重考查酯、过氧键的性质,注意酯基不发生加成反应,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 合成氨生产中将NH3液化分离,虽可提高N2、H2的转化率但减小了反应速率 | |
| B. | 硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 | |
| C. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 | |
| D. | 侯氏制碱法是将氨气和二氧化碳先后通入饱和氯化钠溶液中,制得碳酸氢钠固体,再在高温下灼烧,转化为碳酸钠固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
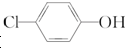 )的废水可以利用微生物电池除去,其原理如图所示,下列说法错误的是( )
)的废水可以利用微生物电池除去,其原理如图所示,下列说法错误的是( )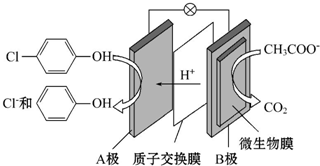
| A. | 该装置能将化学能转化为电能 | |
| B. | A极为正极 | |
| C. | B极上发生氧化反应 | |
| D. | 每有1 mol CH3COO-被氧化,就有8 mol电子通过整个电路 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该锂电池在放电过程中,Li+从正极区向负极区迁移 | |
| B. | 电解质溶液中混入水,对电池反应无影响 | |
| C. | 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 | |
| D. | 电池工作过程中,金属锂提供的电子与正极生成硫的物质的量之比为4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
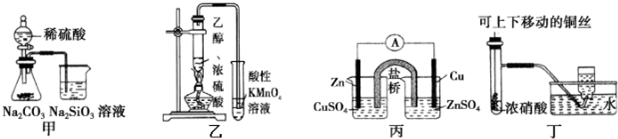
| A. | 图甲证明非金属性强弱:S>C>Si | |
| B. | 装置乙可用于检验有乙烯生成 | |
| C. | 图丙构成铜锌原电池,产生持续稳定的电流 | |
| D. | 图丁可制备并收集NO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下1L 0.1 mol•L-1的FeSO4溶液中含有0.4NA个氧原子 | |
| B. | 用碱性锌锰干电池作电源电解饱和食盐水,当消耗MnO2 8.7g时,可制得标况下氯气2.24L | |
| C. | 1.2g CaCO3与Mg3N2的混合物中含有质子数为0.6NA | |
| D. | 常温下,pH=7的0.5 mol﹒L-1的CH3COONH4溶液中,NH4+浓度为0.5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 仪器用品 |
| A | 准确量取19.01mL水 | 25mL酸式滴定管 |
| B | 新制氯水的保存 | 带玻璃塞的棕色细口瓶 |
| C | 测定0.1mol•L-1的Na2CO3溶液的pH | 镊子、pH试纸、表面皿 |
| D | 分离水和乙酸乙酯 | 分液漏斗、烧杯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com