
| A. | 糖类是有甜的有机物 | |
| B. | 糖类物质又叫碳水化合物,因此所有的糖类均可用通式Cn(H2O)m来表示 | |
| C. | 糖类物质和碳水化合物没有实质的联系 | |
| D. | 糖类可以分为单糖和多糖 |
分析 A.糖类不一定有甜味,如纤维素属于糖但没有甜味;
B.有一部分糖符合Cn(H2O)m的分子通式,但不是所有的糖都符合这个通式;
C.由于最初发现的糖都符合Cn(H2O)m这个通式,所以当时把糖类称为碳水化合物一直沿用至今;
D.糖类可以根据水解情况分为单糖、二糖和多糖;
解答 解:A.糖类不一定有甜味,如纤维素属于糖但没有甜味,故A错误;
B.有一部分糖符合Cn(H2O)m的分子通式,但不是所有的糖都符合这个通式,故B错误;
C.由于最初发现的糖都符合Cn(H2O)m这个通式,所以当时把糖类称为碳水化合物一直沿用至今,故C正确;
D.糖类可以根据水解情况分为单糖、二糖和多糖,故D错误;
故选:C.
点评 本题主要考查糖类的概念和分类,注意对基础知识的理解和运用,题目比较简单.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
| A. | 向NaHCO3溶液中通CO2至pH=7:c(Na+)═c(HCO3-)+c(CO32-) | |
| B. | 向CH3COONa溶液中加入等浓度等体积的盐酸:c(Na+)>c(Cl-) | |
| C. | 向浓度为0.1mol/LNaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH<13 | |
| D. | 将0.1molAgCl投入到100mL0.1mol/LNaCl溶液中:c(Ag+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | CH4 | CH3-CH3 | CH2═CH2 |
| 物质的量分数 | 20% | 30% | 50% |
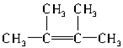 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>W | |
| B. | W的含氧酸的酸性比Z的含氧酸的酸性强 | |
| C. | W的气态氢化物的稳定性小于Y的气态氢化物的稳定性 | |
| D. | 若W与X原子序数差为5,则形成化合物的化学式为X3W2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
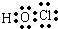 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,加聚反应.
,加聚反应. +3HNO3(浓)$→_{△}^{浓硫酸}$
+3HNO3(浓)$→_{△}^{浓硫酸}$ +3H2O,取代反应.
+3H2O,取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
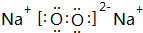
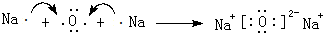 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com