
����Ŀ��[��ѧ����ѡ��5���л���ѧ����]��15�֣� ������G��һ�ֿ���������������ҩ�ʵ�����ɷ�����A�Ʊ�G�ĺϳ�·�����£�
�ش��������⣺
��1��A�Ľṹ��ʽΪ��C�Ļ�ѧ��������
��2���۵ķ�Ӧ�Լ��ͷ�Ӧ�����ֱ��� �� �÷�Ӧ����������
��3���ݵķ�Ӧ����ʽΪ�������һ���л������������
��4��G�ķ���ʽΪ��
��5��H��G��ͬ���칹�壬�䱽���ϵ�ȡ������G����ͬ��λ�ò�ͬ����H���ܵĽṹ���֡�
��6��4-���������������� ![]() ������Ҫ�ľ�ϸ�����м��壬д���ɱ����ѣ�
������Ҫ�ľ�ϸ�����м��壬д���ɱ����ѣ� ![]() ���Ʊ�4-���������������ĺϳ�·���������Լ���ѡ����
���Ʊ�4-���������������ĺϳ�·���������Լ���ѡ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ���NaClO3��ȡClO2���壬����ClO2�Ƶ�NaClO2 �� ʵ��װ����ͼ��ʾ���ش��������⣺ 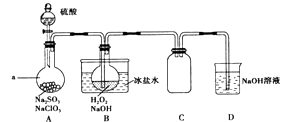
��1������a������Ϊ��װ��C�������� ��
��2����ʵ�����ʹNaClO3��������Ŀ���� ��
��3��ΪʹClO2�����ܱ����ȡ�������գ�����ʱӦע�� ��
��4��NaOH����ClO2β�����������ʵ���֮��Ϊ1��1�����������ӣ�һ��ΪClO2�� �� ����һ��Ϊ ��
��5��B�з�Ӧ�����ӷ���ʽΪ ��
��6��֤��NaClO2���������Եķ����ǣ���B����Һ���ȳ�ȥH2O2 �� ����������ţ���ͬ���ữ���ټ������飮 ��ϡHNO3��ϡH2SO4��K2SO3��Һ ��BaCl2��Һ ��FeCl2��Һ ��KSCN��Һ
��7��Ԥ��NaClO3ת��ΪNaClO2��ת����Ϊ80%����Ҫ�Ƶ�28.9g NaClO23H2O�����������144.5����������g NaClO3�����������106.5����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ� �� 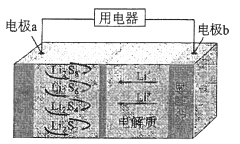
A.��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e-=3Li2S4
B.��ع���ʱ�����·������0.02 mol���ӣ��������ϼ���0.14 g
C.ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D.��س��ʱ��Խ��������е�Li2S2��Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15�֣�
�ظ������һ����Ҫ�Ļ���ԭ�ϣ�һ���ɸ������Ʊ������������Ҫ�ɷ�ΪFeO��Cr2O3 �� �����й衢�������ʡ��Ʊ�������ͼ��ʾ��
�ش��������⣺
��1������ٵ���Ҫ��ӦΪ��
FeO��Cr2O3+Na2CO3+NaNO3 ![]() Na2CrO4+ Fe2O3+CO2+ NaNO2
Na2CrO4+ Fe2O3+CO2+ NaNO2
������Ӧ��ƽ��FeO��Cr2O3��NaNO3��ϵ����Ϊ���ò��費��ʹ���մ�������ԭ������
��2������1�к������Ľ���Ԫ���� �� ����2����Ҫ�ɷ������������ʡ�
��3������ܵ���Һ2��pHʹ֮�������С������ԭ�����������ӷ���ʽ��ʾ����
��4���й����ʵ��ܽ����ͼ��ʾ������Һ3���м�������KCl������Ũ������ȴ�ᾧ�����˵õ�K2Cr2O7���塣��ȴ�������ţ��õ���K2Cr2O7�����Ʒ��ࡣ
a.80�� b.60�� c.40�� d.10��
����ݵķ�Ӧ��������
��5��ij������m1 kg ������ۣ���Cr2O3 40%���Ʊ�K2Cr2O7 �� ���յõ���Ʒ m2 kg������Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����17�֣��Ǽ��㶹����һ�����Ƶ���ʯ��ҩ��ϳ�·������ͼ��ʾ��


��֪�� 
RCOOR'+R'OH ![]() RCOOR'+ R'OH��R��R'��R'����������
RCOOR'+ R'OH��R��R'��R'����������
��1��A���ڷ���������ṹ��ʽ����B�������Ĺ���������
��2��C��D�ķ�Ӧ��������
��3��E����֬�ࡣ�����Ҵ�Ϊ�л�ԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ�E��д���йػ�ѧ����ʽ����
��4����֪��2E ![]() F+C2H5OH��F������������
F+C2H5OH��F������������ ![]() ����
����
��5����D��FΪԭ�Ϻϳ��Ǽ��㶹�ط�Ϊ������Ӧ��д���йػ�����Ľṹ��ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15�֣� ���϶������Dzⶨ�������е������ľ��䷽������ԭ������Ũ�����ڴ��������½���Ʒ���л���ת������Σ�������ͼ��ʾװ�ô�����Σ�Ȼ��ͨ���ζ���������֪��NH3+H3BO3=NH3��H3BO3��NH3��H3BO3+HCl= NH4Cl+ H3BO3��
�ش��������⣺
��1��a����������
��2��b�з����������Ƭ��Ŀ������f����������
��3����ϴ������g�м�����ˮ����k1���ر�k2��k3������b������������·��ֹͣ���ȣ��ر�k1��g������ˮ��������c��ԭ��������k2�ŵ�ˮ���ظ�����2~3�Ρ�
��4��������ϴ��g�м������ᣨH3BO3����ָʾ�������������dע��e�����ע������������Һ��������ˮ��ϴd���ر�k1��d�б�������ˮ����k1������b��ʹˮ��������e�� ��d�б�������ˮ��Ŀ������
��e����Ҫ��Ӧ�����ӷ���ʽΪ �� e�����п�˫�㲣��ƿ����������
��5��ȡij�ʰ��ᣨC2H3NO2����Ʒm �˽��вⶨ���ζ�g������Һʱ����Ũ��Ϊmol��L-1������V mL������Ʒ�е�����������Ϊ%����Ʒ�Ĵ��ȡ�%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����칤����ж�����ˮ�����������������������ι���ν֮���裬������������ȼн������ʮ�����ۣ������߰��ۣ�������̣�������ȼ���ף������Ӽ����Ρ�������û���漰���IJ�����
A. ���� B. �ᾧ C. ���� D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Na2SO4��Fe2(SO4)3�Ļ����Һ����Fe3+�����ʵ���Ũ��Ϊ0.4mol/L��SO42-�����ʵ���Ũ��Ϊ0.7mol/L,��û����Һ��Na+�����ʵ���Ũ��Ϊ
A. 0.1mol/L B. 0.15mol/L C. 0.2mol/L D. 0.25mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com