
现有三组混合物:①汽油和氯化钠溶液 ②碘的CCl4溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.萃取、蒸发、分液 B.分液、蒸馏、萃取
C.分液、萃取、蒸馏 D.蒸馏、萃取、分液
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:2014-2015学年北京市昌平区高二上学期期末考试化学试卷(解析版) 题型:填空题
(4分)某同学设计了由乙醇合成乙二醇的路线如下。
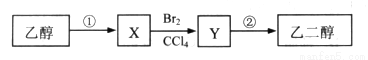
(1)X是 (填名称)。
(2)X→Y的反应类型是 。
(3)写出Y→乙二醇的化学方程式 。
(4)等物质的量的乙醇、乙二醇完全燃烧,消耗氧气的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015天津市和平区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列实验能够证明二氧化硫存在的是
①能使澄清的石灰水变浑浊
②能使湿润的蓝色石蕊试纸变红
③能使湿润的品红试纸褪色
④通入足量的氢氧化钠溶液,再加氯化钡溶液有白色沉淀生成,该沉淀溶于稀盐酸
⑤通入氯水能使氯水褪色,再滴加氯化钡溶液有白色沉淀生成
A.都不能证明 B.③④⑤能证明 C.③⑤能证明 D.只有⑤能证明
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省绵阳市高一上学期期末化学试卷(解析版) 题型:填空题
镁与稀硝酸的反应为:Mg+ HNO3(稀)—— Mg(NO3)2+ NH4NO3+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。
(2)该反应中,还原产物是_________,HNO3表现了________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为________。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省绵阳市高一上学期期末化学试卷(解析版) 题型:选择题
用下图所示装置进行下列实验,实验结果与预测现象不一致的是
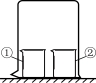
选项 | ①中物质 | ②中物质 | 预测①中现象 |
A | 酚酞溶液 | 浓氨水 | 无色变红色 |
B | 湿润红布条 | 饱和氯水 | 红布条褪色 |
C | 稀氨水 | 浓硝酸 | 溶液变浑浊 |
D | NaAlO2溶液 | 浓盐酸 | 有白色沉淀 |
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省绵阳市高一上学期期末化学试卷(解析版) 题型:选择题
用铜锌合金制成的黄铜制品貌似黄金,下列方法不易区分其真伪的是
A.外观观察 B.放入盐酸中 C.测定密度 D.高温灼烧
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市西城区高三上学期期末考试化学试卷(解析版) 题型:选择题
19.(10分)自然界中氮元素有多种存在形式。
(1)合成氨反应的化学方程式是 。
(2)NH3在一定条件下可被氧化。
已知:ⅰ.4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH=﹣1269 kJ/mol
ⅱ.
① 断开1 mol H-O 键与断开 1 mol H-N 键所需能量相差约______kJ;
② H-O 键比H-N键(填“强”或“弱”)______。
(3)下图是某压强下, N2与H2按体积比1: 3投料时,反应混合物中氨的体积分数随温度的变化曲线。其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。

① 图中b点,U(正)______ U(逆)。(填“>”、“=”或“<”)
② 图中a点,容器内气体n(N2):n(NH3)= 。
(4)水中的氨在微生物作用下可被氧化为亚硝酸,其化学方程式是 。
(5)电解法能将碱性溶液中的NO2转化为N2而除去,其电极反应式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二上学期第二次统练化学试卷(解析版) 题型:填空题
26.(10分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 。
(2)硫酸铜溶液可以加快氢气生成速率的原因是 。
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
混合液 | A | B | C | D | E | F |
4mol·L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1= ,V6= ,V9= 。
②反应一段时间后,实验E中的金属呈 色。
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com