
| 滴定次数 | NaOH溶液体积/mL | 滴定消耗滤液体积/mL |
| 1 | 25.00 | 20.02 |
| 2 | 25.00 | 17.10 |
| 3 | 25.00 | 19.98 |
分析 (1)根据反应物和生成物结合质量守恒定律来书写化学方程式;
(2)根据所配溶液的体积选择容量瓶;
(3)根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(4)先计算NaOH的浓度,由于第二次滴定时数据与另外两次差别较大,舍去,则消耗滤液的体积平均值为$\frac{20.02+19.98}{2}$=20.00mL,根据c(滤液)=$\frac{c(NaOH)V(NaOH)}{V(滤液)}$计算;
(5)俯视标准液液面,则滤液的体积偏小,根据c(滤液)=$\frac{c(NaOH)V(NaOH)}{V(滤液)}$分析误差.
解答 解:(1)TiCl4水解生成TiO2•xH2O,设TiCl4的系数为1,根据元素守恒,TiO2•xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),
故答案为:TiCl4+(x+2)H2O?TiO2•xH2O+4HCl;
(2)配制成250mL溶液使用的量具是250mL容量瓶,故答案为:250mL容量瓶;
(3)酚酞在氢氧化钠溶液中显红色,随着反应进行碱性减弱,溶液颜色变浅,当溶液颜色由粉红色变为无色,且半分钟内不变色,可说明达到滴定终点,
故答案为:浅红色溶液变为无色,且半分钟内不变色;
(4)1.000gNaOH固体质量,配制成250mL溶液,则c(NaOH)=$\frac{n}{V}$=$\frac{\frac{1g}{40g/mol}}{0.25L}$=0.1mol/L,
第二次滴定时数据与另外两次差别较大,舍去,则消耗滤液的体积平均值为$\frac{20.02+19.98}{2}$=20.00mL,
则c(滤液)=$\frac{c(NaOH)V(NaOH)}{V(滤液)}$=$\frac{0.1mol/L×0.025L}{0.02L}$=0.125 mol•L-1,
故答案为:0.125 mol•L-1;
(5)若在滴定终点读取滴定管刻度时,俯视液面,则滴定管中读出的滤液的体积偏小,由c(滤液)=$\frac{c(NaOH)V(NaOH)}{V(滤液)}$可知,计算结果偏大,即测定结果偏高,
故答案为:偏高.
点评 本题考查酸碱中和滴定,明确中和滴定实验的仪器、步骤、终点的判定、数据处理等即可解答,注意滴定管的读数为易错点,题目难度中等.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | K2SO4•2Cr2(SO4)3 | B. | 2K2SO4•Cr2(SO4)3 | C. | K2SO4•Cr2(SO4)3 | D. | K2SO4•$\frac{1}{2}$Cr2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
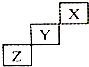
| A. | X是种活泼的非金属元素 | |
| B. | Z的最高价氧化物的水化物是一种弱酸 | |
| C. | Y的氢化物很稳定 | |
| D. | Y元素的最高化合物为+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeCl3溶液 | B. | 溴水 | ||
| C. | 酸性高锰酸钾溶液 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯甲酸的重结晶实验中要得到纯净的苯甲酸固体需要进行两次过滤操作 | |
| B. | 实验室制乙烯时,为减弱浓硫酸对有机物的碳化作用,应用小火缓慢加热 | |
| C. | 在石油的分馏、制硝基苯、制乙烯的实验中,都要使温度计的水银液泡浸入反应液中,以控制实验温度 | |
| D. | 制备硝基苯,混合药品的顺序为:向试管中先加入苯,再加入浓硫酸,最后加入浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学式为CF2Cl2的物质可以看作是甲烷的衍生物,它有两种分子结构 | |
| B. | 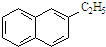 所有原子都处于同一平面 所有原子都处于同一平面 | |
| C. | C3H8O有2种同分异构体 | |
| D. | 甲苯的二氯代物共有10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{n}{16}$ | B. | $\frac{n}{8}$ | C. | 4n | D. | 8n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com