
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届辽宁省分校高三上学期12月月考理综化学试卷(解析版) 题型:选择题
设C+CO2 2CO △H>0反应速率为V1,N2+3H2
2CO △H>0反应速率为V1,N2+3H2 2NH3 △H<0 反应速率为V2,对于上述反应,当温度升高时,V1和V2的变化情况为( )
2NH3 △H<0 反应速率为V2,对于上述反应,当温度升高时,V1和V2的变化情况为( )
A.同时增大 B.同时减小 C.V1 增大,V2减小 D.V1减小,V2增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高一上期中考试化学试卷(解析版) 题型:实验题
某学生欲配制6.0mol/L的H2SO4溶液980mL,实验室有三种不同浓度的硫酸:①480mL 0.5mol/L的硫酸;②150mL 25%的硫酸(ρ=1.18g/mL);③足量的18mol/L的硫酸。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为______________mol/L(保留1位小数)。
(2)该实验需要使用到的玻璃仪器有:量筒、烧杯、玻璃棒、__________、___________。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部倒入烧杯中混合均 匀;
匀;
B.用量筒准确量取所需的18mol/L的浓硫酸,沿烧杯内壁倒入上述混合液中,并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D._______________________________________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧、振荡、摇匀。
(4)如果省略操作D,对所配置溶液浓度有何影响?________(偏大、偏小,无影响?)
(5)进行操作C前还需注意__________________________________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
下列关于水的说法不正确的是( )
A.我们平时应多饮用很纯净的水,防止有毒物质进入体内
B.所有天然水都不能饮用
C.人体内含有约2/3体重的水,故人每天不用喝水也可
D.人类可利用的水只占自然界的水极少量,我们应节约用水
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中理化学试卷(解析版) 题型:选择题
氢氰酸(HCN)的下列性质中,不能证明它是弱电解质的是
A.HCN溶液的导电性比盐酸的弱 B.1mol/LNaCN溶液呈碱性
C.NaCN可以与盐酸反应 D.1mol/LHCN溶液的pH约为3
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖。颁奖理由是“因为发现青蒿素── 一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。”下列关于青蒿素和双氢青蒿素(结构如图)说法错误是
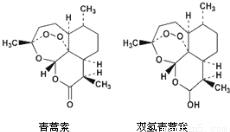
A.青蒿素和双氢青蒿素互为同分异构体
B.由青蒿素制备双氢青蒿素的反应属还原反应
C.青蒿素的分子式为C15H22O5
D.青蒿素分子中含有过氧链和酯基、醚键
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:选择题
某溶液中可能含有OH-、CO32- 、AlO2-、 SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+。当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如图所示,下列说法正确的是
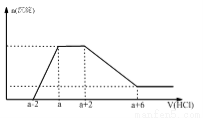
A.原溶液一定含有硫酸钠
B.反应最后形成的溶液中的溶质为氯化钠
C.原溶液中一定含有的阴离子有OH-、CO32- 、AlO2-、 SiO32-
D.原溶液中含有CO32-与AlO2-的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南二校高一理科实验班上联考2化学卷(解析版) 题型:填空题
如表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)③、④、⑦的原子半径由大到小的顺序为 (用元素符号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为 (用酸的化学式表示)。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 ;
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。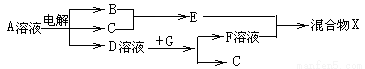
①写出D溶液与G反应的化学方程式 。
②写出检验A溶液中溶质的阴离子的方法 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com