
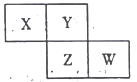
【题目】下图是从元素周期表中截取的一部分,已知X、Y、Z、W为四种短周期主族元素,下列说法正确的是
A. 四种元素的原子有可能均能与氢原子形成18电子分子
B. Z元素可能为金属
C. Z的原子半径不一定比Y的原子半径大
D. W的原子序数不可能是X的原子序数的3倍
【答案】A
【解析】X、Y、Z、W是四种短周期主族元素,根据元素在周期表中的相对位置知,X、Y、Z、W属于第三主族以后的元素,且X和Y位于第二周期、Z和W位于第三周期,如果W是Cl元素,则X、Y、Z分别是N、O、S元素;如果W是S元素,则X、Y、Z分别是C、N、P元素;如果W是P元素,则X、Y、Z分别是B、C、Si元素;A.若X、Y、Z、W分别是N、O、S、Cl元素,那么它们与H原子形成18电子的分子分别是N2H4、H2O2、H2S、HCl,A正确;B.Z可能是S、P、Si元素,所以Z不可能为金属元素,B错误;C.Z位于第三周期,Y位于第二周期,所以Z的原子半径一定比Y的原子半径大,C错误;D.如果W是P、X是B元素,则W原子序数是X的3倍,D错误;答案选A.


科目:高中化学 来源: 题型:
【题目】下列有关描述正确的是( )
A.钠在空气中燃烧,发出淡蓝色的火焰,生成淡黄色固体
B.硅能导电,可用作光导纤维
C.玻璃花瓶和餐桌上的瓷盘都是硅酸盐产品
D.久置的氯水与新制的氯水,都能使有色布条褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据以下信息回答有关问题:
I.NOx是汽车尾气的主要污染物之一。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
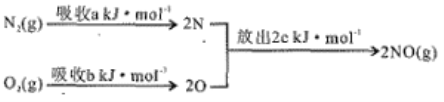
该反应的△H=________________________。
(2)科学家通过实验发现,在紫外线照射下TiO2会使空气中的某些分子产生活性基团OH,并且活性基团OH可与NO2、NO发生反应生成硝酸和水。根据左下图示,请写出OH与NO反应的化学方程式______________________________________。
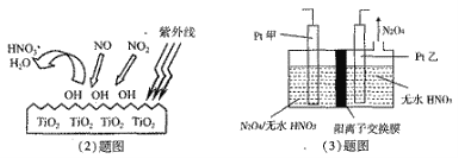
(3)电解法可将工业废气中含有的NO2消除。原理是先将NO2转化为N2O4,然后电解得到N2O5 (常温下为无色固体,常做绿色硝化剂)。电解原理如右上图所示,该电解池中生成N2O5的电极反应式是___________。
Ⅱ为研究哈伯法合成氨反应,T℃时,在容积为2 L恒容容器中通入4 mol N2和12mol H2,反应如下:N2(g)+3H2(g) ![]() 2NH3(g),若25min时反应达到平衡,各物质浓度随时间变化曲线如下图中甲、乙、丙。回答下列问题:
2NH3(g),若25min时反应达到平衡,各物质浓度随时间变化曲线如下图中甲、乙、丙。回答下列问题:
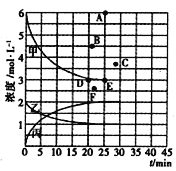
(1)0-25min内,反应的平均速率v(H2)为_________。
(2)T℃时,该反应的平衡常数K=_____________ (用最简分数表达)。
(3)T℃时,若起始充入8mol N2和24 mol H2,则反应刚达到平衡时,表示c( H2)在右图中相应的点为_____(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HNO2的电离平衡常数为K=4.6×10﹣4(已知 ![]() =2.14),向20mL0.01molL﹣1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
=2.14),向20mL0.01molL﹣1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( ) 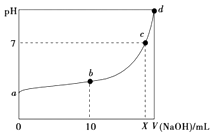
A.HNO2的电离方程式为HNO2=NO2﹣+H+
B.a点H2O电离出的c(H+)=2.14×10﹣3molL﹣1
C.b点溶液中离子浓度大小关系为c(NO2﹣)>c(Na+)>c(H+)>c(OH﹣)
D.X值等于20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种全天候太阳能电池的工作原理如图所示,下列说法正确的是
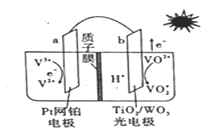
A. 光照时,b极周围pH增大
B. 光照时,H+由a极室透过质子膜进入b极室
C. 夜间无光照时,a极的电极反应式为V2+-e-= V3+
D. 该电池与硅太阳能供电原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火力发电厂释放出的大量NONOx、SO2、CO2会对环境造成污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现节能减排、废物利用等目的.
(1)脱硝:利用甲烷催化还原NOx; CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=﹣574kJmol﹣1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=﹣1160kJmol﹣1
甲烷直接将NO2还原为N2的热化学方程式为 .
(2)脱硫:①某种脱硫工艺将废气处理后可获得硫酸铵和硝酸铵,物质的量浓度相等的硫酸铵溶液和硝酸铵溶液,前者的c(NH4+)与后者的c(NH4+)的关系是 . A.大于2倍 B.等于2倍 C.介于2倍与2倍之间 D.小于1倍
②25℃时pH均为4的硝酸铵溶液和稀硝酸中由水电离出的氢离子浓度分别为c1、c2 , 则c1与c2的比值等于 .
(3)脱碳:废气中的CO2转化为甲醇(CH3OH)可用于制作甲醇燃料电池(结构如图),质子交换膜左右两侧的溶液均为1L2molL﹣1H2SO4溶液.电极c上发生的电极反应式为 , 当电池中有1mole﹣发生转移时左右两侧溶液的质量之差为g (假设反应物a、b耗尽,忽略气体的溶解). 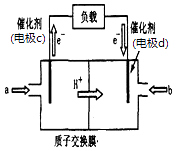
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试分析有机物下列性质中该有机物不具有的是:( ) 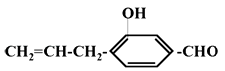 ;(1)加聚反应(2)加成反应 (3)使酸性高锰酸钾溶液褪色(4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应.
;(1)加聚反应(2)加成反应 (3)使酸性高锰酸钾溶液褪色(4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应.
A.(1)(3)
B.(2)(4)
C.(4)
D.(4)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氮的固定是几百年来科学家一直研究的课题 。
下表列举了不冋温度下大气固氮和工业固氮的部分化学平衡常数K的值:
反应 | 大气固氮N2(g)+O2(g) | 工业固氮N2(g)+3H2 (g) | |||
温度/℃ | 27 | 2000℃ | 25 | 400 | 450 |
K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 200 |
①分析数据可知:大气固氮反应属于_____________ (填“吸热”或“放热”反应。
②从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因________________________________。
③在一定的温度和压强下,把2体积N2和6体积H2充入一容积可变的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0。反应达到平衡后N2的质量分数为a%,若在相同容器中充入m 摩尔的N2和n 摩尔的H2也能使平衡时N2的质量分数达到a%,则m 和n 的关系用代数式表达应为___________。若在一定温度下的定容密闭容器中发生上述反应,能说明此反应已达化学平衡状态的是________。
2NH3(g) △H<0。反应达到平衡后N2的质量分数为a%,若在相同容器中充入m 摩尔的N2和n 摩尔的H2也能使平衡时N2的质量分数达到a%,则m 和n 的关系用代数式表达应为___________。若在一定温度下的定容密闭容器中发生上述反应,能说明此反应已达化学平衡状态的是________。
A.密度不变 B.混合气体平均相对分子质量不变
C.V正(N2)= 2v逆(NH3) D.N2的体积分数不再改变
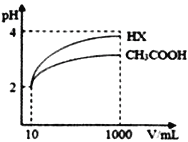
(2)体积均为10mL,pH均为2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH 变化如图:则HX 的电离平衡常数_________(填“大于”、“等于”或“小于”)醋酸的电离平衡常数。稀释后,HX溶液中水电离出来的c (H+)_______ (填“大于”、“等于”或“小于”)醋酸的溶液中水电离出来的c (H+),理由是_______________________________________。
(3)已知100℃时,水的离子积常数为1×10-12,将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a∶b=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表和元素周期律可指导人们进行规律性推测和判断。下列说法中不合理的是
A. 若X+和Y2﹣的核外电子层结构相同,则原子序数:X>Y
B. 硅、锗都位于金属与非金属的交界处,都可以做半导体材料
C. 盐酸(HCl)酸性比H2SiO3强,可推断出元素的非金属性:Cl>Si
D. Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com