
| A. | 氧 | B. | 氮 | C. | 碳 | D. | 氟 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有共价键 | |
| B. | 共价化合物中可能含有离子键 | |
| C. | 第IA族元素与第VIIA族可能形成离子化合物,也可能形成共价化合物 | |
| D. | 非金属元素间不可能形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
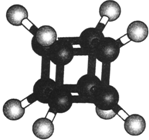
| A. | 它在核磁共振氢谱中只出现一个峰 | |
| B. | 它的二氯代物有两种同分异构体 | |
| C. | 它不易燃烧 | |
| D. | 它与苯乙烯(C6H5-CH═CH2)不是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
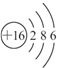 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 弱碱 | B. | 一元强碱 | C. | 多元强碱 | D. | 任何强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
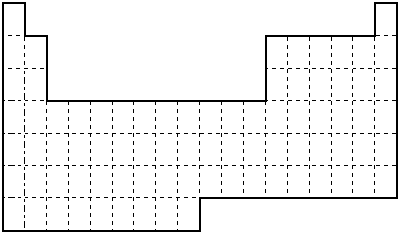
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com