
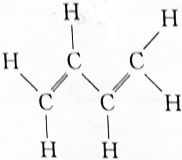
 CH2=CH-CH=CH2、=-=.
CH2=CH-CH=CH2、=-=.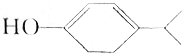 ,则它的分子式为C9H14O,其官能团为羟基和碳碳双键,它属于脂环化合物(填“芳香化合物”或“脂环化合物”)
,则它的分子式为C9H14O,其官能团为羟基和碳碳双键,它属于脂环化合物(填“芳香化合物”或“脂环化合物”) 分析 结构简式是指把分子中各原子连接方式表示出来的式子,通常只适用于以分子形式存在的纯净物.应表现该物质中的官能团:只要把碳氢单键省略掉即可,碳碳单键、碳氯单键、碳和羟基的单键等大多数单键可以省略也可不省略;
键线式中用短线“-”表示化学键,端点、交点表示碳原子,C原子、H原子不需要标出;
据此解答.
解答 解:(1) 的结构简式为CH2=CH-CH=CH2,碳碳双键为官能团不能省略;键线式为:=-=;
的结构简式为CH2=CH-CH=CH2,碳碳双键为官能团不能省略;键线式为:=-=;
故答案为:CH2=CH-CH=CH2;=-=;
(2) 中含有9个C,14个H,1个O,分子式为:C9H14O;官能团为羟基和碳碳双键;含有环,但是不是苯环,所以属于脂环化合物;
中含有9个C,14个H,1个O,分子式为:C9H14O;官能团为羟基和碳碳双键;含有环,但是不是苯环,所以属于脂环化合物;
故答案为:C9H14O;羟基和碳碳双键;脂环化合物;
点评 本题考查了有机化合物表示方法及分类,明确有机化合物结构简式、键线式书写方法是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
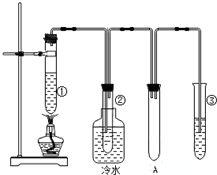 石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已忽略).在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水.
石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已忽略).在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水.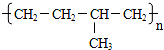 B.
B.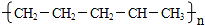
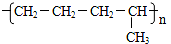 D.
D.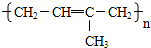
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X单质在一定条件下能与Z的最高价氧化物发生置换反应 | |
| B. | 原子半径:Y>Z>W | |
| C. | 最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W | |
| D. | 室温下,0.1mol/LW的气态氢化物的水溶液的pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 短周期 | ⅠA | ||||||
| ① | |||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||
| ⑦ | ⑧ | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
对于可逆反应 2AB3(g) A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )
A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )
A.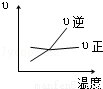 B.
B.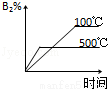 C.
C.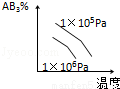 D.
D.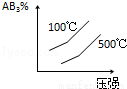
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上10月阶段测化学卷(解析版) 题型:填空题
实验室常用盐酸的质量分数为36.5%,密度为1.20g/㎝3。
(1)此浓盐酸的物质的量浓度是 ?(列式计算)
(2)配制100mL3.00mol/L的盐酸,需以上浓盐酸 mL .(列式计算)
(3)还原4.8g金属氧化物,参加反应的氢气为2.016L(标准状况),生成的金属溶于上述盐酸,放出氢气1.344 L(标准状况),此金属氧化物是 。
A.Fe2O3 B.ZnO C.CuO
(4)将5.0 g CaC O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)
O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)
(5)某金属R与一定体积的上述盐酸正好完全反应所得氯化物溶液20 mL,浓度为0.05 mol/L。它恰好能与20 mL 0.15 mol·L-1 的AgNO3溶液完全反应,则该氯化物的化学式 .
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上10月阶段测化学卷(解析版) 题型:选择题
下列颜色不属于因化学反应而产生的现象的是
A.无色试剂瓶中的浓硝酸呈黄色
B.久置的KI溶液呈黄色
C.新制氯水久置后变为无色
D.在普通玻璃导管口点燃纯净氢气时,火焰呈黄色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com