
设NA为阿伏伽德罗常数。下列叙述正确的是 ( )
A.1mol甲醇中含有C-H键的数目为4NA
B.标准状况下,2.24L已烷含有分子的数目为0.1NA
C.12克金刚石中含有的共价键数目为2NA
D.1 mol 甲基所含的电子数为10NA
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
制印刷电路板时常用FeCl3溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu===2FeCl2+CuCl2,向盛有FeCl3溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是( )
A.烧杯中有铜无铁 B.烧杯中有铁无铜
C.烧杯中铁、铜都有 D.烧杯中铁、铜都无
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.氯气通入水中H2O+ Cl2 2H+ + Cl-+ ClO-
B.氯化铁溶液中加入铁粉2Fe3+ + Fe 3Fe2+
C.碳酸钙加入盐酸中 C032-+2H+=CO2↑+H2O
D.铜片加入稀硝酸中Cu + 2 H+ = Cu2++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
天然橡胶分解后的产物是碳氢化合物,它含C:88.2%,H:11.8%,此气体的相对分子质量是68,求它的化学式。此物质0.5mol能和160gBr2起加成反应,在生成物中溴原子分布在不同的碳原子上,又知溴代物的结构上有一个碳原子是在支链上,根据上述条件写出产物的分子式及结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数。下列叙述正确的是 ( )
A.1mol甲醇中含有C-H键的数目为4NA
B.标准状况下,2.24L已烷含有分子的数目为0.1NA
C.12克金刚石中含有的共价键数目为2NA
D.1 mol 甲基所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
现有等物质的量的铜和银的混合物17.2 g,与50.0 mL
的浓硝酸恰好完全反应,
产生气体4.48 L(标准状况),则下列说法正确的是
A.产生的气体是0.2 mol NO2
B.硝酸的物质的量浓度为12 mol·L-1
C.反应中被还原和未被还原的硝酸物质的量之比为3∶2
D.要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
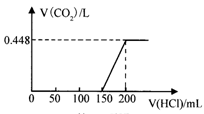
将露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2体积(标准状况)与加入的盐酸体积有如图关系(不考虑CO2在水中的溶解)。试计算:(无需书写计算步骤)
(1)盐酸的物质的量浓度为 mol/L。
(2)该样品中NaOH与Na2CO3物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息判断,下列选项不正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO | Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO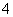 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
中学常见反应的化学方程式有A+B→X+Y+H2O或H2O+ A+B→X+
Y(未配平,反应条件略去),下列问题所涉及反应式中的H2O已经略去。请回答:
(1)常温下,若A为黄绿色气体,B为非金属氧化物,A、B均能使品红溶液褪色,A+B→X+Y,且相对分子质量X>Y,则该反应的化学方程式为________________,检验Y中阴离子的试剂是________________。
(2)若Y是黄绿色气体,且A、B的物质的量之比为1∶4,该反应的化学方程式是 。
(3)若A为常见的金属单质,Y为气态单质,B溶液呈强酸性或强碱性时,A和B反应都能进行。写出A与B反应的离子方程式:_________________;_________________。
(4)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,其中A、B的物质的量之比为1∶4,则反应中氧化剂与还原剂的物质的量之比是 。
(5)若A、B均为化合物,Y为白色沉淀(不含金属元素),B为引起温室效应的主要气体,将B通入某溶液后可生成Y,写出Y可能的化学式______________。写出生成Y的一个离子方程式______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com