


 »ĘøŌ¹Ś¾üæĪæĪĮ·ĻµĮŠ“š°ø
»ĘøŌ¹Ś¾üæĪæĪĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢BµÄ×Ŗ»ÆĀŹ½µµĶ |
| B”¢Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ |
| C”¢x+y£¼z |
| D”¢CµÄĢå»ż·ÖŹżĻĀ½µ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £¬ĘäÖŠ±ūŹĒČÜÓŚĖ®ĻŌĖįŠŌµÄĘųĢ壬¶”ŹĒĒæ¼ī£®
£¬ĘäÖŠ±ūŹĒČÜÓŚĖ®ĻŌĖįŠŌµÄĘųĢ壬¶”ŹĒĒæ¼ī£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ¶ĢÖÜĘŚŌŖĖŲÖĆX”¢Y”¢R”¢QŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠQŌŖĖŲŹĒµŲæĒÖŠŗ¬Įæ×īøßµÄŌŖĖŲ£®
¶ĢÖÜĘŚŌŖĖŲÖĆX”¢Y”¢R”¢QŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠQŌŖĖŲŹĒµŲæĒÖŠŗ¬Įæ×īøßµÄŌŖĖŲ£®| ÅضČ/mol?L-1 Ź±¼ä/min |
NO | N2 | RO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 35 | 0.32 | 0.34 | 0.15 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
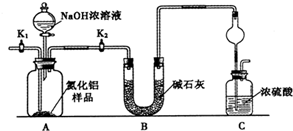
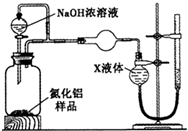
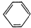
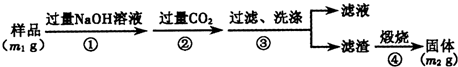
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ŃĻ½ūŌŚ¼ÓÓĶÕ¾ø½½üČ¼·ÅŃĢ»Ø±¬Öń |
| B”¢½šŹōÄĘŅāĶā×Å»šŹ±£¬Į¢¼“ÓĆÕ“Ė®µÄĆ«½ķø²øĒ |
| C”¢µ±ÓŠ“óĮæĀČĘųŠ¹Ā©Ź±£¬ČĖÓ¦ŃŲĖ³·ē·½ĻņŹčÉ¢ |
| D”¢½«ŗ¬ÓŠĮņĖįµÄ·ĻŅŗµ¹ČėĖ®³Ų£¬ÓĆ“óĮæĖ®³åČėĻĀĖ®µĄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢¼ÓČėÉŁĮæĀČ»Æ¼Ų¹ĢĢå |
| B”¢¼ÓČėÉŁĮæĀČ»ÆĢś¹ĢĢå |
| C”¢¼õÉŁFe£ØSCN£©3µÄÅØ¶Č |
| D”¢¼ÓĖ®Ļ”ŹĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| A”¢Ptµē¼«ŹĒøĆ×°ÖƵÄÕż¼« |
| B”¢øƵē³Ų·¢ÉśµÄÕż¼«·“Ó¦ĪŖ£ŗO2+4e-+2H2O=4OH- |
| C”¢øŗ¼«µÄµē¼«·“Ó¦Ź½£ŗNO-2e-+O2-=NO2 |
| D”¢¹ĢĢåµē½āÖŹÖŠO2-Ļņøŗ¼«ŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com