
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
分析 (1)由元素在周期表中位置,可知①为C、②为F、③为Mg、④为Al、⑤为Si、⑥为S、⑦为Cl、⑧为Ar、⑨为K、⑩为Br;
(2)同周期自左而右金属性减弱,同主族自上而下金属性增强;碳元素组成有机物,形成的化合物种类最多;
(3)氢氧化铝是两性氢氧化物,⑥、⑨最高价氧化物的水化物分别为硫酸、KOH,氢氧化铝与硫酸发生中和反应生成硫酸铝与水,氢氧化铝与氢氧化钾反应生成偏铝酸钾与水;
(4)利用单质之间的相互置换反应等可以说明非金属性强弱.
解答 解:(1)由元素在周期表中位置,可知①为C、②为F、③为Mg、④为Al、⑤为Si、⑥为S、⑦为Cl、⑧为Ar、⑨为K、⑩为Br,
故答案为:Si;Ar;
(2)同周期自左而右金属性减弱,同主族自上而下金属性增强,故表中K元素的金属性最强,碳元素组成有机物,形成的化合物种类最多,
故答案为:钾;碳;
(3)Al元素的氢氧化物--氢氧化铝是两性氢氧化物,⑥、⑨最高价氧化物的水化物分别为硫酸、KOH,氢氧化铝与硫酸发生中和反应生成硫酸铝与水,反应方程式为:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O,氢氧化铝与氢氧化钾反应生成偏铝酸钾与水,反应方程式为:Al(OH)3+KOH=KAlO2+2H2O,
故答案为:Al;2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O;Al(OH)3+KOH=KAlO2+2H2O;
(4)利用单质之间的相互置换反应等可以说明非金属性强弱,反应方程式为:Cl2+Na2S═2NaCl+S↓,
故答案为:Cl2+Na2S═2NaCl+S↓.
点评 本题考查元素周期表与元素周期律综合应用,比较基础,有利于基础知识的巩固,注意金属性、非金属性强弱比较实验事实.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 要鉴别的物质组 | 试剂 | 方法 |
| A | NaCl/Na2CO3 | BaCl2溶液 | 观察是否产生沉淀 |
| B | NO2/Br2 | 湿润的淀粉碘化钾试纸 | 观察试纸是否变蓝色 |
| C | 乙醇/乙酸 | 新制氢氧化铜悬浊液 | 观察溶液是否变澄清 |
| D | CO2/SO2 | 品红溶液 | 观察溶液红色是否退去 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
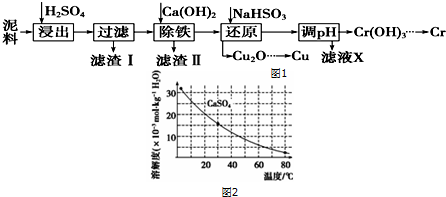
| 物质 | Fe3+ | Cu2+ | Cr3+ |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.5g | B. | 13.2g | C. | 19.7g | D. | 24.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Cl | B. | CHCl3 | C. | CCl4 | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用澄清石灰水鉴别CO2和SO2 | |
| B. | 用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 用CO2鉴别NaAlO2溶液和NaClO溶液 | |
| D. | 用Ba(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X 的简单气态氢化物的热稳定性比W 的弱 | |
| B. | 原子半径的大小顺序:rY>rZ>rW>rX | |
| C. | 化合物YX、ZX2、WX3 中化学键的类型相同 | |
| D. | 最高价氧化物对应水化物的酸性:W比Z 的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子内共价键越强,分子越稳定,其熔沸点也越高 | |
| B. | 离子键的本质就是阴、阳离子之间的相互吸引 | |
| C. | 变化过程中化学键被破坏,则一定发生化学变化 | |
| D. | 由原子构成的晶体可能是原子晶体,也可能是分子晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com