


 .
.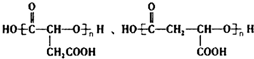 .
. )与F的相对分子质量相同,其中满足下列条件的X的同分异构体有14种(含X本身).
)与F的相对分子质量相同,其中满足下列条件的X的同分异构体有14种(含X本身). 的最简合成线路.
的最简合成线路.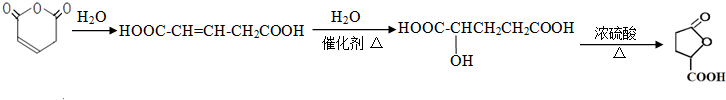 .
. 分析 A是一种五元环状化合物,A能水解生成B,B能和氢气发生加成反应生成C,结合题给信息和A的分子式知,A中还含有碳碳双键,则A的结构简式为: ,故B为HOOCCH=CHCOOH,C为HOOCCH2CH2COOH,C和与D反应生成E,根据E的分子式知,D是CH3CH2OH,E的结构简式为CH3CH2OOCCH2CH2COOCH2CH3.B和水发生反应生成F,所以F为HOOCCH2CH(OH)COOH,F发生缩聚反应得到高聚物G为
,故B为HOOCCH=CHCOOH,C为HOOCCH2CH2COOH,C和与D反应生成E,根据E的分子式知,D是CH3CH2OH,E的结构简式为CH3CH2OOCCH2CH2COOCH2CH3.B和水发生反应生成F,所以F为HOOCCH2CH(OH)COOH,F发生缩聚反应得到高聚物G为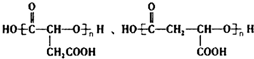 ,有机物Y(C5H4O3)是A的同系物,具有六元环结构,则Y为
,有机物Y(C5H4O3)是A的同系物,具有六元环结构,则Y为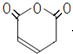 ,由Y合成
,由Y合成 可以用
可以用 先发生水解生成HOOCCH2CH=CHCOOH,HOOCCH2CH=CHCOOH再与水发生加成反应生成HOOCCH2CH2CHOHCOOH,HOOCCH2CH2CHOHCOOH再发生分子内脱水反应可得
先发生水解生成HOOCCH2CH=CHCOOH,HOOCCH2CH=CHCOOH再与水发生加成反应生成HOOCCH2CH2CHOHCOOH,HOOCCH2CH2CHOHCOOH再发生分子内脱水反应可得 ,据此答题.
,据此答题.
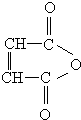
解答 解:A是一种五元环状化合物,A能水解生成B,B能和氢气发生加成反应生成C,结合题给信息和A的分子式知,A中还含有碳碳双键,则A的结构简式为: ,故B为HOOCCH=CHCOOH,C为HOOCCH2CH2COOH,C和与D反应生成E,根据E的分子式知,D是CH3CH2OH,E的结构简式为CH3CH2OOCCH2CH2COOCH2CH3.B和水发生反应生成F,所以F为HOOCCH2CH(OH)COOH,F发生缩聚反应得到高聚物G为
,故B为HOOCCH=CHCOOH,C为HOOCCH2CH2COOH,C和与D反应生成E,根据E的分子式知,D是CH3CH2OH,E的结构简式为CH3CH2OOCCH2CH2COOCH2CH3.B和水发生反应生成F,所以F为HOOCCH2CH(OH)COOH,F发生缩聚反应得到高聚物G为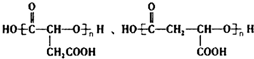 ,
,
(1)A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)B为HOOCCH=CHCOOH,所含官能团的名称是:羧基、碳碳双键,
故答案为:羧基、碳碳双键;
(3)反应③的化学方程式为:2CH3CH2OH+HOOCCH2CH2COOH $→_{△}^{浓硫酸}$CH3CH2OOCCH2CH2COOCH2CH3+2H2O,该反应为取代反应,物质E为CH3CH2OOCCH2CH2COOCH2CH3,有3种化学环境不同的H原子,核磁共振氢谱上有3个峰,
故答案为:2CH3CH2OH+HOOCCH2CH2COOH $→_{△}^{浓硫酸}$CH3CH2OOCCH2CH2COOCH2CH3+2H2O;取代反应;3;
(4)高分子化合物G的结构简式可能为: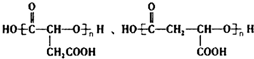 ,
,
故答案为: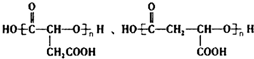 ;
;
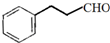
(5)与F相对分子质量相同的有机物X( )有多种同分异构体,其同分异构体中含苯环且能发生银镜反应,含有醛基,则符合条件的结构可以是苯环上连有1个侧链为-CH2CH2CHO,或者为-CH(CH3)CHO,可以是苯环上连有有2个侧链为-CH2CHO、-CH3,或者-CH2CH3、-CHO,各有邻、间、对3种;
)有多种同分异构体,其同分异构体中含苯环且能发生银镜反应,含有醛基,则符合条件的结构可以是苯环上连有1个侧链为-CH2CH2CHO,或者为-CH(CH3)CHO,可以是苯环上连有有2个侧链为-CH2CHO、-CH3,或者-CH2CH3、-CHO,各有邻、间、对3种;
可以是苯环上连有有3个侧链为-CHO、2个-CH3,2个-CH3处于邻位时,-CHO有2种位置,2个-CH3处于间位时,-CHO有3种位置,2个-CH3处于对位时,-CHO有1种位置,
故符合条件的同分异构体有2+6+2+3+1=14种,
故答案为:14;
(6)有机物Y(C5H4O3)是A的同系物,具有六元环结构,则Y为 ,参照上述合成线路及信息,由Y合成
,参照上述合成线路及信息,由Y合成 可以用
可以用 先发生水解生成HOOCCH2CH=CHCOOH,HOOCCH2CH=CHCOOH再与水发生加成反应生成HOOCCH2CH2CHOHCOOH,HOOCCH2CH2CHOHCOOH再发生分子内脱水反应可得
先发生水解生成HOOCCH2CH=CHCOOH,HOOCCH2CH=CHCOOH再与水发生加成反应生成HOOCCH2CH2CHOHCOOH,HOOCCH2CH2CHOHCOOH再发生分子内脱水反应可得 ,合成路线为
,合成路线为 ,
,
故答案为: ;
;
点评 本题考查有机物推断、有机反应类型、官能团、同分异构体等,关键是推断A的结构,注意利用有机物分子式与反应条件进行推断,明确有机物的断键和成键方式是解决有机题的关键,难度中等.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:解答题
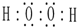 ;肼的结构式
;肼的结构式 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
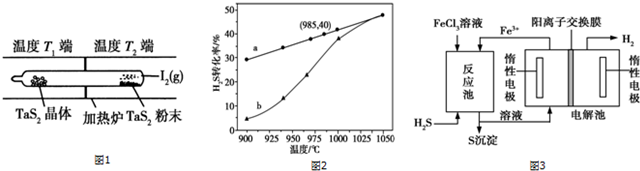
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应A(g)?2B(g)△H,若正反应的活化能为Ea kJ/mol,逆反应的活化能为Eb kJ/mol,则△H=-( Ea-Eb)kJ/mol | |
| B. | 常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同 | |
| C. | 某温度氯化钠在水中的溶解度是20 g,该温度饱和氯化钠溶液的质量分数为20% | |
| D. | 将浓度为0.1 mol/L HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Z>G>M>Y | |
| B. | X、M形成的简单阴离子的还原性:X>M | |
| C. | G与Y形成的化合物一定既能与盐酸反应,又能与烧碱溶液反应 | |
| D. | X、Z分别与Y可形成原子数为1:1的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ─CH3+6KMnO4→3
─CH3+6KMnO4→3 ─COOK+6MnO2+3KOH+3H2O
─COOK+6MnO2+3KOH+3H2O ─COOK+HCl→
─COOK+HCl→ ─COOH+KCl
─COOH+KCl| 名称 | 相对分子质量 | 性状 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |

 ,操作Ⅱ为蒸馏.
,操作Ⅱ为蒸馏.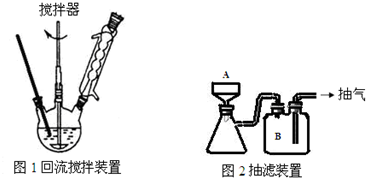
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H10的属于烷烃的同分异构体有3种 | |
| B. | 分子组成是C5H10属于烯烃的同分异构体有6种 | |
| C. | 分子组成是C4H8O属于醛类的同分异构体有3种 | |
| D. | 结构为 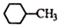 的物质的一溴代物有5种 的物质的一溴代物有5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com