
���� ��1��������13�����ӣ�����13�ֲ�ͬ�˶�״̬���ݴ���д�۲�����Ų��������ж��ٸ������ӣ����ж����ֲ�ͬ�˶�״̬��
��2�����Ӿ�����۷е�ϵͣ�Fe��CO��5�к���6���Ҽ���2���м����ȵ�������ԭ�����ͼ۵���������ͬ��
��3������ԾǨ�ͷŵĹ��ܣ�ʹ����ʱ��������������ɫ��
��4��ͬһ���ڣ�Ԫ�صĵ�һ����������ԭ����������������������ƣ�����IIA��͵�VA��Ԫ�ش���������Ԫ�ص�һ�����ܣ�ͬһ����Ԫ�أ�Ԫ�صĵ�һ����������ԭ���������������С��SO42-��Sԭ�ӵļ۲������Ϊ4�������ӻ��������Ϊsp3��SO42-�Ŀռ乹��Ϊ���������Σ�����ԭ��ΪCu�ļ۲������Ϊ4�������ӻ��������Ϊsp3��
��5����������������ÿ��Feԭ����Χ��8��Feԭ�ӣ���������������ÿ��Cuԭ����Χ��12��Feԭ�ӣ���������λ��֮��Ϊ8��12=2��3���������������߳�Ϊapm�����V=a3������Feԭ����ĿΪ8��$\frac{1}{8}$+1=2����a3�ѣ����ģ�=2��$\frac{56}{NA}$���������������߳�Ϊbpm�����V=b3������Cuԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4����b3�ѣ����ģ�=4��$\frac{64}{NA}$���ʦѣ����ģ����ѣ����ģ�=7b3��16a3���ݴ˽��з�����
��� �⣺��1��Cu�ĺ��������Ϊ29����Cu+�ĺ��������Ϊ28���۲������Ϊ10���ʼ۲�����Ų�ͼΪ3d10����Ԫ�ص�ԭ������Ϊ26����̬Fe3+�ĵ����Ų�ʽΪ1s22s22p63s23p63d5�����京��23���˶�״̬��ͬ�ĵ��ӣ�
�ʴ�Ϊ��3d10��23��
��2��������һ�������Fe��CO��5�۵�Ϊ-20.5�棬�е�Ϊ103�棬������CCl4�����ݷ��Ӿ�����������ʣ����Ӿ����۷е�ͣ��������л��ܼ����������ڷ��Ӿ��壻Fe��CO��5�к���6���Ҽ���2���м����ʦҼ���м�����Ŀ֮��Ϊ3��1��N2��CN-��CO��ԭ��������2���۵���������10����Ϊ�ȵ����壬
�ʴ�Ϊ�����Ӿ��壻3��1��CN-��
��3��ͭԪ�ص���ɫ��Ӧ����ɫ���ܶ����Ԫ���ܷ�����ɫ��Ӧ����ԭ��Ϊ������ԾǨ�ͷŵĹ��ܣ�ʹ����ʱ��������������ɫ��
�ʴ�Ϊ������ԾǨ�ͷŵĹ��ܣ�ʹ����ʱ��������������ɫ��
��4��ͬһ���ڣ�Ԫ�صĵ�һ����������ԭ����������������������ƣ�����IIA��͵�VA��Ԫ�ش���������Ԫ�ص�һ�����ܣ�ͬһ����Ԫ�أ�Ԫ�صĵ�һ����������ԭ���������������С�����Էǽ���Ԫ��H��O��S��N�ĵ�һ�������ɴ�С��˳����H��S��O��N��SO42-��Sԭ�ӵļ۲������Ϊ4�������ӻ��������Ϊsp3��SO42-�Ŀռ乹��Ϊ���������Σ�����ԭ��ΪCu�ļ۲������Ϊ4�������ӻ��������Ϊsp3��
�ʴ�Ϊ��H��S��O��N�����������Σ�sp3��
��5����������������ÿ��Feԭ����Χ��8��Feԭ�ӣ���������������ÿ��Cuԭ����Χ��12��Feԭ�ӣ���������λ��֮��Ϊ8��12=2��3���������������߳�Ϊapm�����V=a3������Feԭ����ĿΪ8��$\frac{1}{8}$+1=2����a3�ѣ����ģ�=2��$\frac{56}{NA}$���������������߳�Ϊbpm�����V=b3������Cuԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4����b3�ѣ����ģ�=4��$\frac{64}{NA}$���ʦѣ����ģ����ѣ����ģ�=7b3��16a3��
�ʴ�Ϊ��2��3��7b3��16a3��
���� �����Ƕ����ʽṹ�Ŀ��飬�漰��������Ų��������ܡ��ȵ����塢�ӻ���ʽ����������ȣ�ע�������̯�����о����йؼ��㣬����ͬ���ڵ�һ�������쳣������Ѷ��еȣ�


 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 48 mol•��L•s ��-1 | B�� | 36 mol•��L•s ��-1 | C�� | 24 mol•��L•s ��-1 | D�� | 12 mol•��L•s ��-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 60g�����д��ڵĹ��ۼ�����Ϊ10NA | |
| B�� | 92g�Ҵ��������Ľ����Ʒ�Ӧ������������H2���ķ�����ΪNA | |
| C�� | ��״���£�22.4L������̼̼����ĿΪ5NA | |
| D�� | ��ϩ�ͼ��ѵĻ���ﹲ0.1mol����ȫȼ�������ĵ���������һ��Ϊ0.6NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20% | B�� | 33% | C�� | 50% | D�� | 89% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
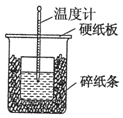 50mL 0.55mol•L-1������50mL 0.50mol•L-1NaOH��Һ����ͼ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
50mL 0.55mol•L-1������50mL 0.50mol•L-1NaOH��Һ����ͼ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
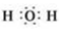 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe | B�� | Al | C�� | Al2O3 | D�� | Si |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��Һϴ��ʱ������Ӧ�����ӷ���ʽΪ��2OH-+Cl2=Cl-+ClO-+H2O | |
| B�� | ����ʵ����Եó����������£�������Cl2��O2 | |
| C�� | ����ʵ����Եó���Ӧ���Ũ�Ⱥ���Һ��pH��Ӱ�����ʵ������� | |
| D�� | ����·��ͨ��2mol����ʱ���������ռ�����״�����������Ϊ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ�n����ʱ��/min | ||
| CO | H2O | CO2 | ||||
| 1 | 500 | 8 | 4 | 3.2 | 4 | |
| 2 | 700 | 4 | 2 | 0.8 | 3 | |
| 3 | 700 | 4 | 2 | 0.8 | 1 | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com