
| A. | 原子半径:r(X)>r(R)>r(W) | |
| B. | X与Y只能形成一种化合物 | |
| C. | X的简单气态氢化物的热稳定性比Z的弱 | |
| D. | 由W、R、X三种元素组成的化合物可以是酸、碱或盐 |
分析 W、R、X、Y、Z是原子序数依次增大的短周期主族元素.Y原子半径在短周期主族元素中最大,Y为Na元素;W与Y同主族,W为H或Li元素;R原子最外层电子数比内层电子数多3,则R的最外层电子数为5,R为N元素;X与Z同主族,W、Y原子的电子数总和与X、Z原子的电子数总和之比为1:2,设X的电子数为n,则(1+11):(n+n+8)=1:2,解得n=8,即X为O,Z为S,或(3+11):(n+n+8)=1:2,解得n=10与主族元素不符,则W只能为H,以此来解答.
解答 解:由上述分析可知,W为H,R为N,X为O,Y为Na,Z为S,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:r(R)>r(X)>r(W),故A错误;
B.X与Y能形成H2O、H2O2,故B错误;
C.非金属性X>Z,X的简单气态氢化物的热稳定性比Z的强,故C错误;
D.由W、R、X三种元素组成的化合物可以是酸、碱或盐,如硝酸、一水合氨、硝酸铵,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质、原子结构来推断元素为解答的关键,侧重分析与推断能力的考查,注意Y为Na及规律性知识的应用,选项D为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
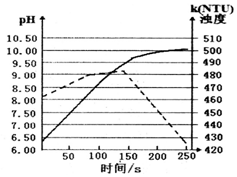 将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )
将打磨后的镁条放入盛有50mL蒸馏水的烧杯中,用pH传感器和浊度传感器监测溶液中pH和溶液浊度随时间的变化如图.下列有关描述正确的( )| A. | 该实验是在常温下进行的 | |
| B. | 实线表示溶液浊度随时间的变化 | |
| C. | 50s时向溶液中滴入酚酞试液,溶液变红 | |
| D. | 150s后溶液浊度下降是因为生成的Mg(OH)2沉降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯酸甲酯和甲醇 | B. | 对硝基甲苯和含硝酸的水层 | ||
| C. | 硝酸钾和氯化钠 | D. | 氯化铵和碳酸铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知25℃时NH4CN溶液显碱性,则25℃时的电离常数K(NH3•H2O)>K(HCN) | |
| B. | 室温时,相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO2-4且浓度均为0.010 mol•L-1溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO2-4先产生沉淀 | |
| D. | 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
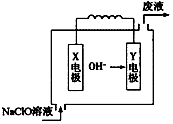 镁是一种重要的金属资源,在各领域都具有重要的作用.
镁是一种重要的金属资源,在各领域都具有重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性强弱:F2>Cl2>Br2 | B. | 非金属性:O>S>Se | ||
| C. | 还原性强弱:F->Cl->I- | D. | 碱性强弱:KOH>NaOH>LiOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com