
| A、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B、化学反应中的能量变化都表现为热量变化 |
| C、△H的大小与热化学方程式的计量数无关 |
| D、生成物的总焓大于反应物的总焓时,反应吸热,△H>0 |


科目:高中化学 来源: 题型:
| A、对于0.1 mol?L-1 Na2SO3溶液中:2c (Na+)═c(SO32-)+c(HSO3-)+c(H2SO3) |
| B、将CH3COOK溶液和盐酸溶液混合所得中性溶液:c(K+)>c(Cl-)=c(CH3COOH) |
| C、Ka(CH3COOH)=1.8×10-5,Ka(HCN)=4.9×10-10,物质的量浓度相同的CH3COONa、NaCN溶液中:c(CH3COO-)>c(CN-) |
| D、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤的干馏是物理变化,煤的气化和液化是化学变化 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、沼气(主要成分是CH4)是可再生能源 |
| D、太阳能、氢能、风能、地热能、生物质能都是新能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 | B、5 | C、9 | D、12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、p(H2)>p(O2)>p(Ar) |
| B、p(O2)>p(Ar )>p(H2) |
| C、p(Ar)>p(H2)>p(O2) |
| D、p(H2)>p(Ar)>p(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ?mol-,则氢气的标准燃烧热为-241.8 kJ?mol-11 |
| B、已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| C、已知2C(s)+2O2(g)=2CO2(g)△H=a2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D、已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
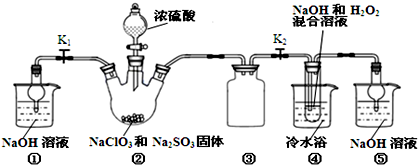
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com