
·ÖĪö £Ø1£©ŅĄ¾ŻČܶȻż³£ŹżøÅÄīŹéŠ“±ķ“ļŹ½£»
£Ø2£©ĀČ»ÆĆ¾Ė®½āÉś³ÉĒāŃõ»ÆĆ¾ŗĶĀČ»ÆĒā£»
£Ø3£©³żČ„MgCl2ĖįŠŌČÜŅŗÖŠÉŁĮæµÄFeCl3£¬ĄūÓĆ¼ÓČėµÄŹŌ¼Įµ÷½ŚČÜŅŗPHŹ¹ĢśĄė×ÓĶźČ«³Įµķ£¬Ķ¬Ź±²»ÄÜŅżČėŠĀµÄŌÓÖŹ£»
£Ø4£©ČōŌŚæÕĘųÖŠ¼ÓČČMgCl2•6H2O£¬æÉÉś³ÉMg£ØOH£©Cl»ņMgO£¬ŅĄ¾ŻŌ×ÓŹŲŗćŹéŠ“»Æѧ·½³ĢŹ½£»
£Ø5£©ĀČ»ÆĆ¾Ė®½āĻŌĖįŠŌ£¬ĀČ»ÆĒāĘųĮ÷ÖŠ¼ÓČČ·ĄÖ¹Ė®½ā£»
£Ø6£©ŅĄ¾Żµē½āŌĄķŹéŠ“µē¼«·“Ó¦£»
½ā“š ½ā£ŗ£Ø1£©ŅĄ¾ŻČܶȻż³£ŹżøÅÄīŹéŠ“±ķ“ļŹ½£¬Mg£ØOH£©2£Øs£©?Mg2+£Øaq£©+2OH-£Øaq£©£¬Ksp=c£ØMg2+£©•c2£ØOH-£©£»
¹Ź“š°øĪŖ£ŗc£ØMg2+£©•c2£ØOH-£©£»
£Ø2£©ĀČ»ÆĆ¾Ė®½āÉś³ÉĒāŃõ»ÆĆ¾ŗĶĀČ»ÆĒā£¬Mg2++2H2O?Mg£ØOH£©2+2H+£¬¹Ź“š°øĪŖ£ŗMg2++2H2O?Mg£ØOH£©2+2H+£»
£Ø3£©³żČ„MgCl2ĖįŠŌČÜŅŗÖŠÉŁĮæµÄFeCl3£¬ĄūÓĆ¼ÓČėµÄŹŌ¼Įµ÷½ŚČÜŅŗPHŹ¹ĢśĄė×ÓĶźČ«³Įµķ£¬Ķ¬Ź±²»ÄÜŅżČėŠĀµÄŌÓÖŹ£»
a£®MgOæÉŅŌŗĶĖį·“Ó¦µ÷½ŚČÜŅŗPHŹ¹ĢśĄė×Ó³Įµķ£¬²»ŅżČėŠĀµÄŌÓÖŹ£¬¹Źa·ūŗĻ£»
b£®Mg£ØOH£©2 ŗĶĖį·“Ó¦µ÷½ŚČÜŅŗPHŹ¹ĢśĄė×Ó³Įµķ£¬²»ŅżČėŠĀµÄŌÓÖŹ£¬¹Źb·ūŗĻ£»
c£®MgCO3 ŗĶĖį·“Ó¦µ÷½ŚČÜŅŗPHŹ¹ĢśĄė×Ó³Įµķ£¬²»ŅżČėŠĀµÄŌÓÖŹ£¬¹Źc·ūŗĻ£»
d£®MgSO4ŗĶĖį²»·“Ó¦£¬²»Äܵ÷½ŚČÜŅŗPHŹ¹ĢśĄė×Ó³Įµķ£¬ŅżČėŠĀµÄŌÓÖŹĄė×ÓĮņĖįøłĄė×Ó£¬¹Źd²»·ūŗĻ£»
¹Ź“š°øĪŖ£ŗabc£»
£Ø4£©ČōŌŚæÕĘųÖŠ¼ÓČČMgCl2•6H2O£¬æÉÉś³ÉMg£ØOH£©Cl»ņMgO£¬ŅĄ¾ŻŌ×ÓŹŲŗćŹéŠ“»Æѧ·½³ĢŹ½ĪŖ£ŗMgCl2•6H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$Mg£ØOH£©Cl+HCl”ü+5H2O”ü»ņMgCl2•6H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$MgO+2HCl”ü+5H2O”ü£»
¹Ź“š°øĪŖ£ŗMgCl2•6H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$Mg£ØOH£©Cl+HCl”ü+5H2O”ü»ņMgCl2•6H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$MgO+2HCl”ü+5H2O”ü£»
£Ø5£©ĀČ»ÆĆ¾Ė®½āĻŌĖįŠŌ£¬ĀČ»ÆĒāĘųĮ÷ÖŠ¼ÓČČ·ĄÖ¹Ė®½ā£¬HClĘųĮ÷æÉŅÖÖĘMg2+Ė®½ā£»
¹Ź“š°øĪŖ£ŗHClĘųĮ÷æÉŅÖÖĘMg2+Ė®½ā£»
£Ø6£©ŅĄ¾Żµē½āŌĄķŹéŠ“µē¼«·“Ó¦£¬µē½āČŪČŚµÄMgCl2£¬ĀČĄė×ÓŅĘĻņŃō¼«Ź§µē×ÓÉś³ÉĀČĘų£¬Ć¾Ąė×ÓŌŚŅõ¼«µĆµ½µē×ÓÉś³ÉĆ¾£¬Ńō¼«µÄµē¼«·“Ó¦ĪŖ£»2Cl--2e-=Cl2”ü£»¹Ź“š°øĪŖ£ŗ2Cl--2e-=Cl2”ü£®
µćĘĄ ±¾Ģāæ¼²éĮĖŗ£Ė®ĢįČ”Ć¾µÄ¹¤ŅµÉś²śĮ÷³Ģ·ÖĪöÅŠ¶Ļ£¬³żŌÓŹŌ¼ĮŃ”ŌńŌŌņ£¬µē½āŌĄķµÄ·ÖĪöÓ¦ÓĆ£¬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ÆѧĆū³ĘĪŖŅŅ“¼ | B£® | Ņ×»Ó·¢ | ||
| C£® | ³£ÓĆ×÷ÓŠ»śČܼĮ | D£® | ²»Äܱ»ĖįŠŌøßĆĢĖį¼ŲŃõ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
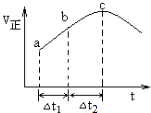
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ČÜÖŹ | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A£® | ÉŁĮ涞Ńõ»ÆĢ¼ĶØČėNaClOČÜŅŗÖŠ£ŗ2NaClO+CO2+H2O”śNa2CO3+2HClO | |
| B£® | ¹żĮæµÄ HCNµĪČėĢ¼ĖįÄĘČÜŅŗÖŠ HCN+Na2CO3”śNaCN+NaHCO3 | |
| C£® | ½įŗĻÖŹ×ÓÄÜĮ¦ÓÉĒæµ½ČõµÄĖ³ŠņĪŖ£ŗHCO3-£¾CN-£¾C6H5O- | |
| D£® | ³£ĪĀĻĀµēĄė³£Źż£ŗKa2£ØH2CO3£©£¾Ka£ØC6H5OH£©£¾Ka £ØHCN£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
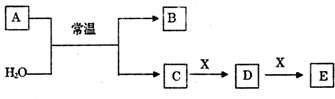
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįøĘŹÜČČ·Ö½ā | B£® | ŅŅ“¼Č¼ÉÕ | ||
| C£® | ŃĪĖįÓėĒāŃõ»ÆÄĘÖŠŗĶ | D£® | Ńõ»ÆøĘČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | O2£¬O3£¬O4 | B£® | 40Ca£¬40Ar | C£® | Fe2+£¬Fe3+ | D£® | ė£¬ė®£¬ė° | ||||
| E£® | H2O£¬D2O£¬T2O | F£® | H2£¬D2£¬T2 | G£® | Na£¬Na+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
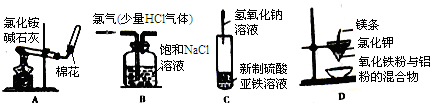
| A£® | ŹµŃéŹŅÖĘČ”²¢ŹÕ¼Æ°±Ęų | B£® | ³żČ„Cl2ÖŠµÄHClĘųĢåŌÓÖŹ | ||
| C£® | ŹµŃéŹŅÖĘČ”ĒāŃõ»ÆŃĒĢś | D£® | ĀĮČČ·“Ó¦ŹµŃé |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com