

| A、现象3不能证明X中是否含有SO42- |
| B、现象2气体C中至少有一种是CO2或SO2,操作Ⅰ为过滤 |
| C、现象5表明X溶液中一定含有Cl- |
| D、现象1表明X溶液显酸性,沉淀D为Fe(OH)3 |


科目:高中化学 来源: 题型:
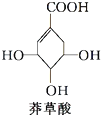 莽草酸是目前世界上被证明是对抗禽流感的唯一良方--“达菲”的原材料,其结构简式如图,下列关于莽草酸的说法正确的是( )
莽草酸是目前世界上被证明是对抗禽流感的唯一良方--“达菲”的原材料,其结构简式如图,下列关于莽草酸的说法正确的是( )| A、分子式为C7H6O5 |
| B、该化合物可以与FeCl3溶液发生显色反应 |
| C、可发生加成和取代反应 |
| D、在水溶液中羧基和羟基均能电离出H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
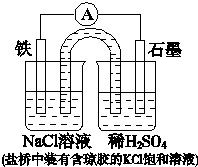
| A、Fe作正极,发生氧化反应 |
| B、负极反应:2H++2e-=H2↑ |
| C、工作一段时间后,NaCl溶液中c(Cl-)增大 |
| D、工作一段时间后,两烧杯中溶液pH均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向无色溶液中加氯水变橙色,溶液中可能含:SO42-,Br-,OH-,Ba2+ |
| B、在c(H+)=10-14mol/L的溶液中可能含:Na+,AlO2-,CO32-,SO32- |
| C、某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3- |
| D、使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Ca2+,HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由“BF3和SO3互为等电子体”,可推知二者均为非极性分子 |
| B、由“同主族元素性质相似,CO2为直线形分子”,可推知SiO2为直线形分子 |
| C、由“SiH4的熔沸点比CH4高”,可推知PH3的熔沸点比NH3高 |
| D、由“C、N、O三种元素的电负性C<N<O”,可推知第一电离能C<N<O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热方能发生的反应一定是吸热反应 |
| B、1molH2SO4和1mol Ba(OH)2完全反应放出的热量叫中和热 |
| C、反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小 |
| D、原电池是将电能转化为化学能的一种装置 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com