
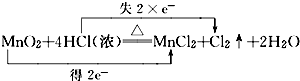 ;
; ;
;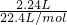 =0.1mol,被氧化的HCl中Cl元素生成氯气,根据氯原子守恒,被氧化的HCl物质的量为:0.1mol×2=0.2mol;
=0.1mol,被氧化的HCl中Cl元素生成氯气,根据氯原子守恒,被氧化的HCl物质的量为:0.1mol×2=0.2mol; 分析操作对所配溶液浓度的影响;
分析操作对所配溶液浓度的影响; 理解溶液的配制与误差分析.
理解溶液的配制与误差分析. 

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
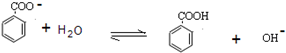
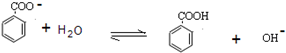
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源:2013届江苏省泰州中学高三上学期期中考试化学试卷(带解析) 题型:实验题
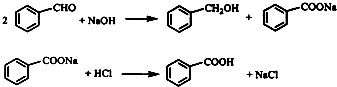
实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸,反应式如下: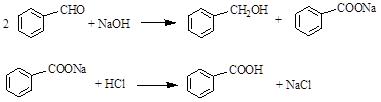
已知:①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃)
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83%~48.0%时易发生爆炸

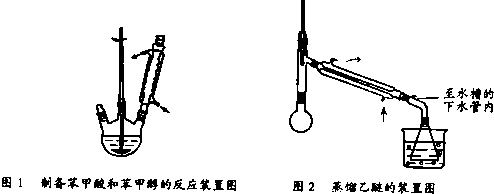
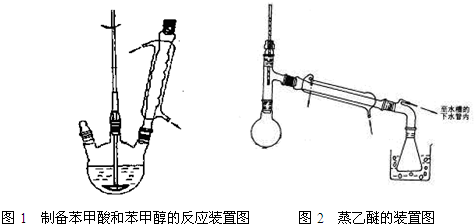
图1 制备苯甲酸和苯甲醇的反应装置图 图2 蒸乙醚的装置图
实验步骤如下:
①向图1所示装置中加入8g氢氧化钠和30mL水,搅拌溶解。稍冷,加入10 mL新蒸过的苯甲醛。开启搅拌器,调整转速,使搅拌平稳进行。加热回流约40 min。
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温。反应物冷却至室温后,倒入分液漏斗,用乙醚萃取三次,每次10mL。水层保留待用。合并三次萃取液,依次用5 mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10 mL水洗涤。
③分出醚层,倒入干燥的锥形瓶,加无水硫酸镁,注意锥形瓶上要加塞。将锥形瓶中溶液转入图2所示蒸馏装置,缓缓加热。升高温度蒸馏,当温度升到140℃时改用空气冷凝管,收集198℃~204℃的馏分得产品A。将萃取后的水溶液慢慢地加入到盛有30 mL浓盐酸和30 mL水的混合物中,同时用玻璃棒搅拌,析出白色固体。冷却,抽滤,得到粗产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)步骤①中所加的苯甲醛为什么要是新蒸的?_____________________________________。
(2)步骤②萃取时用到的玻璃仪器除了除烧杯、玻璃棒外,还需______________________,饱和亚硫酸氢钠溶液洗涤是为了除去__________________,而碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸。
(3)步骤③中无水硫酸镁的作用是_________________,将锥形瓶中溶液转入图2所示蒸馏装置时涉及的实验操作为__________________。
(4)产品A为____________,蒸馏除乙醚的过程中采用的加热方式为_______________,提纯产品B所用到的实验操作为________________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省宿州市高一上学期期末考试化学试卷(解析版) 题型:填空题
实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)反应物中,氧化剂是________;化合价升高的元素是________。
(2)取一定体积的浓盐酸与MnO2发生反应,产生的氯气在标准状况下的体积为1.12 L(忽略Cl2的溶解)。则参加反应的HCl的物质的量是________;反应中被氧化的HCl的质量是________。(写出简要解题过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
I .如下图所示,A、B、C是实验室常用的三种制取气体的装置,提供的药品有:大理石、浓盐酸、稀盐酸、锌粒、二氧化锰、氯化铵、熟石灰.现欲利用这些药品分别制取NH3、Cl2、H2、CO2四种气体,试回答以下问题.
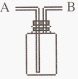
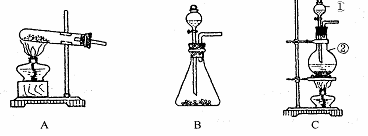
(1) 选用A装置可制取的气体有 ,选用B装置可制取的气有 ,
通常选用C装置制取的气体有 。
(2) 写出利用上述有关药品制取氨气的化学方程式: 。
若要制得干燥的氨气,可选用下列干燥剂中的 (填序号)
a. 生石灰 b. 浓硫酸 C. 五氧化二磷 d. .碱石灰
II. (3) 实验室制取的一氧化氮气体利用右图装置选用必要试剂如何进行收集?
。
III.(4) 现安装一套实验室利用液一液反应制备气体的装置。有人设计了五步操作,请你安排出正确而简捷的程序,将序号填入括号内。
( )将蒸馏烧瓶固定在铁架台上。
( )把酒精灯放在铁架台上,根据酒精灯确定铁圈的高度,固定铁圈,放好石棉网。
( )用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集器中。
( )检查装置的气密性(利用对固定装置进行微热的方法来检查气密性,假定瓶口漏气而需要更换橡皮塞)。
( )在蒸馏烧瓶上装好分液漏斗,连接好导气管。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com