
【题目】下列变化与氧化还原反应无关的是( )
A.向FeCl3溶液中滴加KSCN溶液,溶液变红
B.金属钠投入水中,有气体产生
C.将盛有氯气的试管倒扣在水中,水位上移
D.向H2S溶液中通入SO2气体,产生淡黄色沉淀
【答案】A
【解析】
氧化还原反应的本质是有电子的转移,特征是有化合价的变化。
A.向FeCl3溶液中滴加KSCN溶液,Fe3+与SCN-发生络合反应:Fe3++3SCN-= Fe (SCN)3,该反应没有化合价变化,不是氧化还原反应,A符合题意;
B.金属钠投入水中:2Na+2H2O = 2NaOH+H2↑,Na与H有化合价变化,是氧化还原反应,B不符合题意;
C.将盛有氯气的试管倒扣在水中:Cl2+H2O![]() HCl+HClO,Cl的化合价变化,是氧化还原反应,C不符合题意;
HCl+HClO,Cl的化合价变化,是氧化还原反应,C不符合题意;
D.向H2S溶液中通入SO2气体:2H2S+SO2=3S↓+2H2O,S的化合价变化,是氧化还原反应,D不符合题意;
故选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A. CCl4的比例模型:
B. 对甲基苯酚的结构简式:![]()
C. 乙醛的结构简式:C2H4O
D. 乙醇分子的比例模型:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种红棕色金属氧化物,B、D是金属单质。
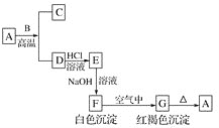
(1)写出下列物质的化学式:A________、E________、F________、G________。
(2)按要求写方程式:
①A+B→C+D的化学方程式:_________________________________;
②F→G的化学方程式:________________________________________________;
③E→F的离子方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中物质的量浓度为1mol/L的是( )
A.将40g NaOH溶解在1L水中
B.将22.4L HCl气体溶于水配成1L溶液
C.将1L 10 mol/L浓盐酸加入9L水中
D.将10g NaOH溶于少量水,在稀释到溶液为250ml
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表述不正确的是( )
A.电解CuCl2溶液:Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
B.NaCl的形成过程:![]()
C.HCl在水中电离:HCl=H++Cl-
D.NH4Cl在水中发生水解:NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其分子结构示意图如图。W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。(注:实线代表共价键,其他重复单元的W、X未标注)下列说法不正确的是( )
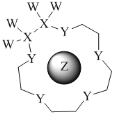
A.Y单质的氧化性在同主族中最强
B.离子半径:Z>Y
C.Z与Y可组成多种离子化合物
D.氢化物的热稳定性:Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,不能达到相应实验目的的是( )
选项 | ① | ② | ③ | 实验目的 |
|
A | 稀硫酸 | Na2S | AgCl的浊液 | 验证Ag2S比AgCl难溶 | |
B | 浓硝酸 | Cu片 | NaOH溶液 | 探究浓硝酸具有氧化性 | |
C | 硫酸 | Na2SO3 | 酸性KMnO4溶液 | 探究SO2具有还原性 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 验证酸性:硝酸>碳酸>硅酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油炼制过程中产生的H2S是一种有毒气体,其有效利用是亟需解决的问题。
(1)H2S的电子式是_________。
(2)热分解法处理H2S
H2S(g)=H2(g)+S(s) ΔH1
已知:i.2H2S(g)+SO2(g)=3S(s)+2H2O(l) ΔH2
ii.S(s)+O2(g)=SO2(g) ΔH3
①利用ΔH2和ΔH3计算ΔH1时,还需要利用_______反应的ΔH。
②直接加热分解H2S转化率低,科学家发现MoS2可以催化H2S分解制取氢气和硫磺,多孔陶瓷膜可以使氢气选择性分离。科学家使用沉积有MoS2的多孔陶瓷膜装置进行反应的原因有_________。
(3)电化学法处理H2S
为避免硫磺沉积在阳极,将氧化吸收和电解制氢过程分开进行,装置如图所示。氧化吸收器中为Fe2(SO4)3溶液,电解反应器中,以石墨为阳极,以Pt为阴极,中间用质子交换膜隔开。
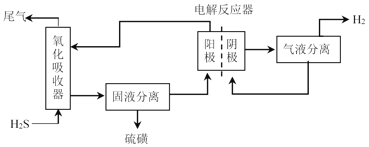
①氧化吸收器中反应的离子方程式为_________。
②电解反应器中,阴极的电极反应式为_________。
③电解反应器的作用是_________(写出2点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

Ⅰ.若X、Y是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞。
(1)写出电解饱和食盐水的离子方程式____;
(2)在X极附近观察到的现象是____。
Ⅱ.若用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
(1)X电极电极反应式是____,Y电极的材料是___;
(2)当电路中有0.04mol电子通过时,阴极增重___g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com