
【题目】化合物F是一种食品保鲜剂,可按如下途径合成:
 已知:RCHO+CH3CHO
已知:RCHO+CH3CHO![]() RCH(OH)CH2CHO。
RCH(OH)CH2CHO。
试回答:
(1)A的化学名称是_________,A→B的反应类型是_________。
(2)B→C反应的化学方程式为_____________________________。
(3)C→D所用试剂和反应条件分别是_____________。
(4)E的结构简式是______________。F中官能团的名称是________________。
(5)连在双键碳上的羟基不稳定,会转化为羰基,则D的同分异构体中,只有一个环的芳香族化合物有______种。其中苯环上只有一个取代基,核磁共振氢谱有5个峰,峰面积比为2∶1∶2∶2∶1的同分异构体的结构简式为______________。
(6)写出用乙醇为原料制备2-丁烯醛的合成路线(其他试剂任选):_____________。
【答案】对二甲苯(或1, 4-二甲苯)取代反应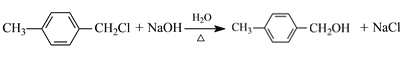 O2/Cu或Ag,加热(或答氧气,催化剂、加热)
O2/Cu或Ag,加热(或答氧气,催化剂、加热)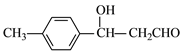 碳碳双键、醛基8
碳碳双键、醛基8![]() ,
,![]()
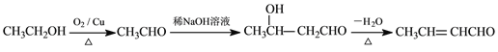
【解析】
由流程转化关系,结合题给信息可知,D为![]() 。运用逆推法, C为
。运用逆推法, C为![]() ,催化氧化生成
,催化氧化生成![]() ;B为
;B为![]() ,在氢氧化钠溶液中,共热发生水解反应生成
,在氢氧化钠溶液中,共热发生水解反应生成![]() ;A为
;A为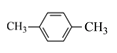 ,在光照条件下与氯气发生侧链的取代反应生成
,在光照条件下与氯气发生侧链的取代反应生成![]() ;
;![]() 与乙醛发生信息反应生成
与乙醛发生信息反应生成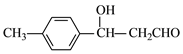 ,
,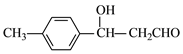 加热发生消去反应生成
加热发生消去反应生成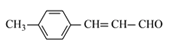 。
。
(1)A的结构简式为 ,名称为对二甲苯;A→B的反应为
,名称为对二甲苯;A→B的反应为 在光照条件下与氯气发生侧链的取代反应生成
在光照条件下与氯气发生侧链的取代反应生成![]() 。B→C反应为
。B→C反应为![]() 在氢氧化钠溶液中,共热发生水解反应生成
在氢氧化钠溶液中,共热发生水解反应生成![]() ,反应的化学方程式为:
,反应的化学方程式为: 。(4)C→D的反应为
。(4)C→D的反应为![]() 在铜或银作催化剂,在加热条件下与氧气发生氧化反应生成
在铜或银作催化剂,在加热条件下与氧气发生氧化反应生成![]() 。(5)
。(5)![]() 与乙醛发生信息反应生成
与乙醛发生信息反应生成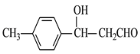 ,则E的结构简式为
,则E的结构简式为 ;
; 的官能团为碳碳双键和醛基。(5)D的同分异构体中,只有一个环的芳香族化合物说明侧链为链状结构,其可能为醛、酮、含苯环的乙烯基醚和乙烯基酚,其中芳香醛有3种(除去D)、芳香酮1种、含苯环的乙烯基醚1种、乙烯基酚3种,共8种;苯环上只有一个取代基,核磁共振氢谱有5个峰,峰面积比为2∶1∶2∶2∶1的同分异构体的结构简式为
的官能团为碳碳双键和醛基。(5)D的同分异构体中,只有一个环的芳香族化合物说明侧链为链状结构,其可能为醛、酮、含苯环的乙烯基醚和乙烯基酚,其中芳香醛有3种(除去D)、芳香酮1种、含苯环的乙烯基醚1种、乙烯基酚3种,共8种;苯环上只有一个取代基,核磁共振氢谱有5个峰,峰面积比为2∶1∶2∶2∶1的同分异构体的结构简式为![]() 和
和![]() 。(6)由题给信息,结合逆推法可知乙醇催化氧化生成乙醛,乙醛在氢氧化钠溶液中发生信息反应生成
。(6)由题给信息,结合逆推法可知乙醇催化氧化生成乙醛,乙醛在氢氧化钠溶液中发生信息反应生成![]() ,
,![]() 加热脱水生成2-丁烯醛,合成路线为:
加热脱水生成2-丁烯醛,合成路线为: 。
。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯(柠檬烯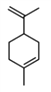 )。提取柠檬烯的实验操作步骤如下:
)。提取柠檬烯的实验操作步骤如下:
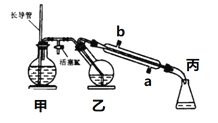
(1)将1~2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30 mL水
(2)松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。
下列说法不正确的是( )
A. 当馏出液无明显油珠,澄清透明时,说明蒸馏完成
B. 蒸馏结束后,为防止倒吸,立即停止加热
C. 长玻管作安全管,平衡气压,防止由于导管堵塞引起爆炸
D. 要得到纯精油,还需要用到以下分离提纯方法:萃取、分液、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一铁、铜混合物粉末平均分成三等份,分别加入到同浓度、不同体积的稀硝酸中,充分反应后,收集到NO气体的体积及剩余固体的质量如表 (设反应前后溶液的体积不变,气体体积已换算为标准状况时的体积):
实验序号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
1 | 100 | 17.2 | 2.24 |
2 | 200 | 8.00 | 4.48 |
3 | 400 | 0 | V |
下列说法正确的是( )
A. 表中V=7.84 L
B. 原混合物粉末的质量为25.6 g
C. 原混合物粉未中铁和铜的物质的量之比为2:3
D. 实验3所得溶液中硝酸的物质的量浓度为0.875 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室中发现了一瓶无色、有刺激性气味的气体,根据气味判断可能是氨气,但不能确定一定是氨气。下列提供的方法中,你认为能够帮他检验是否为氨气的是
A. 将湿润的红色石蕊试纸放在打开的瓶口
B. 将湿润的蓝色石蕊试纸放在打开的瓶口
C. 用蘸有浓硫酸的玻璃棒靠近打开的瓶口
D. 用干燥的红色石蕊试纸放在打开的瓶口
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
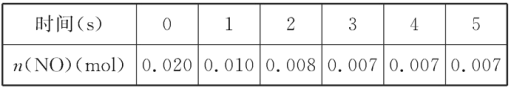
(1)上述反应____(填“是”或“不是”)可逆反应,在第5s时,NO的转化率为________。
(2)如图中表示NO2变化曲线的是____。用O2表示从0s~2s内该反应的平均速率v=_______。
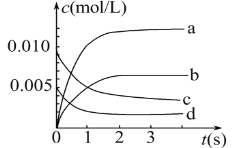
(3)能说明该反应已达到平衡状态的是_______。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v[(NO)逆]=2v[(O2)正] d.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.钠在空气中燃烧最后所得产物为过氧化钠
B.镁在空气中能稳定存在,是因为其表面形成了致密的氧化膜
C.铝制品在生活中非常普遍,这是因为铝不活泼
D.铁不能形成致密的氧化膜,在潮湿的空气中易生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷的浓硫酸。某兴趣小组的同学发现:将一定量的生铁与浓硫酸加热时,观察到固体能完全溶解,并产生大量气体。为探究反应后的产物,请你协助他们完成相关的实验。
[探究一]
(1)另称取铁钉(碳素钢)6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要判断溶液X中是否含有Fe2+,应选用____
a.KSCN溶液和氯水 b.K3[Fe(CN)6]溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学将336mL(标准状况)气体Y通入足量溴水中,发现溶液颜色变浅,试用化学方程式解释溴水颜色变浅的原因:_________________________________________________,然后向反应后的溶液中加入足量BaCl2溶液,经适当操作得干燥固体2.33g。由此推知气体Y中SO2的体积分数为_________。
[探究二]
分析上述实验中SO2体积分数的结果,两同学认为气体Y中还可能含有H2和Q气体。为此设计如图所示探究实验装置(图中夹持仪器省略)。
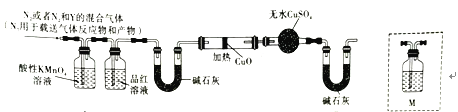
(2)装置A中发生反应的离子方程式为___________,装置B中试剂的作用是____________。
(3)认为气体Y中还含有气体Q的理由是_______________(用化学方程式表示)。为了进一步确认Q的存在,需在装置中添加装置M于______(填序号),M中所加试剂为______。
a.A~B之间 b.B~C之间 c.C~D之间 d.E~F之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预测原子序数为114的元素,具有相当稳定性的同位素,它的位置在第7周期IVA族,称为类铅。关于它的性质,预测错误的是
A. 它的最外层电子数为4 B. 它的金属性比铅强
C. 它具有+2、+4价 D. 它的最高价氧化物的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以含有Ca2+、Mg2+、Cl-、SO![]() 、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
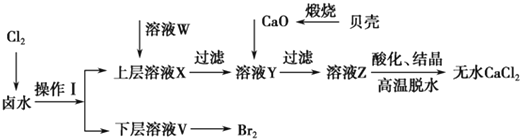
(1)操作Ⅰ使用的试剂是____________,所用主要仪器的名称是________。
(2)加入溶液W的目的是______________。用CaO调节溶液Y的pH,可以除去Mg2+。由表中数据可知,理论上可选择的pH最大范围是____________。酸化溶液Z时,使用的试剂为__________。
开始沉淀时的pH | 沉淀完全时的pH | |
Mg2+ | 9.6 | 11.0 |
Ca2+ | 12.2 | c(OH-)=1.8 mol·L-1 |
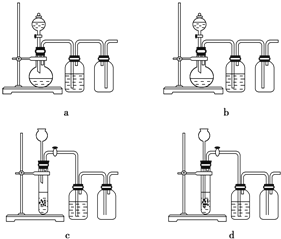
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是__________。
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3的酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于___________________________。用一个化学方程式表示H2SO3酸性强于H2CO3: __________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com