
| A. | 无色溶液中可能大量存在:Al3+、NH4+、S2-、Cl- | |
| B. | 酸性溶液中可能大量存在:I-、ClO-、SO42-、Na+ | |
| C. | 中性溶液中可能大量存在:SO42-、K+、Fe3+、Cl- | |
| D. | 弱碱性溶液中可能大量存在:Na+、K+、Cl-、HCO3- |
分析 A.铝离子与硫离子发生双水解反应;
B.次氯酸根离子能够氧化碘离子,次氯酸根离子与氢离子反应;
C.铁离子只能存在于酸性溶液;
D.四种离子之间不反应,且能够存在于弱碱性溶液中.
解答 解:A.Al3+、S2-之间发生双水解反应,在溶液中不能大量共存,故A错误;
B.酸性溶液中存在大量氢离子,I-、ClO-之间发生氧化还原反应,ClO-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Fe3+水解溶液呈酸性,溶液不可能呈中性,故C错误;
D.Na+、K+、Cl-、HCO3-之间不反应,能够存在于碱性溶液中,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池属于二次电池,在充电过程中,阳极质量减小,阴极质量增加 | |
| B. | 常温下,能自发进行的反应,△H一定小于“0” | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的活化能 | |
| D. | 相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由元素X与Z形成的化合物中只含共价键 | |
| B. | XY2、ZY2、M2Y2的晶体分别属于3种不同类型的晶体 | |
| C. | 单质M的晶体是体心立方堆积,M的配位数是8 | |
| D. | X的氢化物X2H2分子中含有2个σ键和3个π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
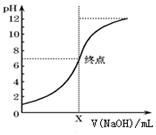 某学生用0.10mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂.重复上述滴定操作2~3 次,记录数据如下.
某学生用0.10mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂.重复上述滴定操作2~3 次,记录数据如下.| 数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 23.40 |
| 第二次 | 25.00 | 4.00 | 23.90 |
| 第三次 | 25.00 | 5.00 | 25.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 c1<c2 | B. | c1>c2 | C. | c1=c2 | D. | 2 c1=c2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com