

| A. | S(s,单斜)=S(s,正交)△H=+0.33kJ/mol | |
| B. | 正交硫比单斜硫稳定 | |
| C. | 相同物质的量的正交硫比单斜硫所含有的能量高 | |
| D. | 1molSO2(g)分解成lmol S(s,单斜)和lmol O2(g)时会放出热量 |
分析 由图象可以看出,单斜硫的能量比正交硫的能量高,物质的能量越高越不稳定,生成SO2的反应为放热反应,以此解答该题.
解答 解:A.单斜硫的能量比正交硫的能量高,S(s,单斜)=S(s,正交)△H=-0.33kJ/mol,为放热反应,故A错误;
B.物质的能量越高越不稳定,则正交硫比单斜硫稳定,故B正确;
C.由图象可以看出,单斜硫的能量比正交硫的能量高,故C错误;
D.互为逆过程的反应的焓变互为相反数,即1molSO2(g)分解成lmol S(s,单斜)和lmol O2(g)时会吸收的能量,故D错误.
故选B.
点评 本题考查化学反应与能量的变化,题目难度不大,注意分析能量曲线,判断反应热、活化能与键能的关系.


科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:K+、Na+、Fe2+、SO42- | |
| B. | 在碱性溶液中:Ba2+、Na+、SO42-、Cl- | |
| C. | 加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ | |
| D. | 含大量Fe3+溶液中:K+、Cl-、SO42-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸不能存放于玻璃瓶中 | |
| B. | 氯水存放于棕色试剂瓶中 | |
| C. | 少量金属钠保存在煤油中 | |
| D. | 氢氧化钠溶液存放于玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 反应叙述 | 产物图示 |
| A | NaOH溶液与SO2 反应时溶液中的溶质 |  |
| B | NaAlO2溶液与盐酸反 应后铝元素的存在形式 |  |
| C | Fe和稀HNO3反应 后,铁元素的存在形式 | 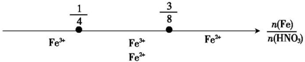 |
| D | Fe在Cl2中的燃烧产物 |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 不小心将少量浓硫酸沾到皮肤,立即用水冲洗 | |
| B. | 如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液 | |
| C. | 为了避免浪费,应该把实验用剩的药品放回原试剂瓶中 | |
| D. | 连接并组装成套仪器时,一般按自下而上、从左到右的顺序进行安装 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7, K2=5.6×l0-11 |
| A. | CH3COO-、CO32-、CN-在溶液中可以大量共存 | |
| B. | 向食醋中加入水可使CH3COOH的电离平衡向电离方向移动 | |
| C. | 相同物质的量浓度的Na2CO3和NaCN溶液,前者pH较大 | |
| D. | pH=a的上述3种酸溶液,加水后溶液的pH相同,则醋酸中加入的水最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min n/mol | 0min | 2min | 4min | 6min | 8min |
| n(X) | 0.2 | 0.15 | 0.1 | 0.1 | 0.05 |
| n(Y) | 0.6 | 0.45 | 0.3 | 0.3 | 0.5 |
| n(Z) | 0 | 0.1 | 0.2 | 0.2 | 0.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com