
| A.降低温度 | B.增大压强 | C.减少NH3 | D.使用催化剂 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 达到平衡。
达到平衡。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 qZ(g) △H=" +Q" kJ·mol—1(Q>0),下列叙述正确的是( )
qZ(g) △H=" +Q" kJ·mol—1(Q>0),下列叙述正确的是( )| A.反应达到最大限度时,加入X,反应的△H增大 | |
| B.在一定条件下向容器中放入m molX和n mol Y,充分反应吸收Q kJ的能量 | |
C.反应速率υ正(X) = υ正(Y) υ正(Y) | D.降低温度,反应的速率值变大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.红棕色的NO2加压后颜色先变深再变浅 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.合成氨时采用循环操作,可提高原料的利用率 |
| D.打开汽水瓶,看到有大量的气泡逸出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
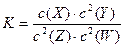 ,有关该平衡体系的说法正确的是 ( )
,有关该平衡体系的说法正确的是 ( )| A.升高温度,平衡常数K一定增大 |
| B.增大压强,W(g)质量分数增加 |
C.该反应的化学反应方程式为X+2Y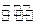 2Z+2W 2Z+2W |
| D.增大X(g)浓度,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 R(g)+S(g)在体积和温度不变的密闭容器中进行。下列事实中,可作为反应达到化学平衡状态的标志的是。
R(g)+S(g)在体积和温度不变的密闭容器中进行。下列事实中,可作为反应达到化学平衡状态的标志的是。| A.单位时间内生成n mol Q的同时生成n mol R |
| B.单位时间内生成n mol R 的同时生成n mol S |
| C.反应器内P、Q、R、S四种气体物质的量浓度相等 |
| D.反应器内P、Q、R、S四种气体共存 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
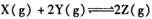 一定达到化学平衡状态的是
一定达到化学平衡状态的是| A.①②③ | B.②③④ | C.②④⑤ | D.①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com