
【题目】某化学兴趣小组为验证SO2的还原性和Fe3+的氧化性,特邀你参与以下探究活动。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的
(1)确定选择SO2和FeCl3溶液的反应而不选择SO2和Fe(NO3)3溶液的反应来探究,你认为可能是基于什么原因作出的选择:_______________________________________。
(2)将SO2通入FeCl3溶液中,你认为可能观察到的现象是:______________________,你预测的理论依据是(用离子方程式表示):___________________________________。
II.实验探究
(1)配制1mol·L-1FeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:_________。
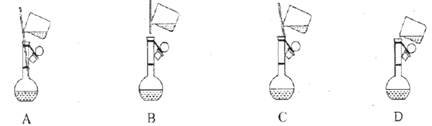
②检测得知溶液呈酸性,其原因是:___________________________(用离子方程式表示)。
(2)将SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知:[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:_____________________________________。
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2,溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。请你推测小组在实验方案设计中“加浓HCl酸化”的目的是:_____________________________________________________。
【答案】NO3-可能对验证Fe3+的氧化性有干扰 溶液由(棕)黄色变为浅绿色 2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42 + 4H+ A Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+ FeCl3+ SO2 + H2O
Fe(OH)3 + 3H+ FeCl3+ SO2 + H2O ![]() [Fe(HSO3)]Cl2 + HCl 增大H+浓度,使“ FeCl3+ SO2 + H2O
[Fe(HSO3)]Cl2 + HCl 增大H+浓度,使“ FeCl3+ SO2 + H2O ![]() [Fe(HSO3)]Cl2 + HCl”平衡逆向移动,加快预期反应的速率
[Fe(HSO3)]Cl2 + HCl”平衡逆向移动,加快预期反应的速率
【解析】
本题考查SO2和FeCl3溶液反应的实验探究,涉及物质性质的分析,物质的量浓度溶液的配制,盐类的水解,外界条件对化学平衡的影响,结合相应知识进行分析;
I.(1)SO2溶于水显酸性,酸性条件下, NO3-也可将SO2氧化,干扰实验,因此,本题答案为:NO3-可能对验证Fe3+的氧化性有干扰;
(2)由于SO2具有还原性,Fe3+具有氧化性,预测SO2通入FeCl3溶液中SO2将Fe3+还原为Fe2+,可能观察到的现象是:溶液由棕黄色变为浅绿色。反应的离子方程式可表示为SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,因此,本题答案为:溶液由(棕)黄色变为浅绿色 ;2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42 + 4H+ ;
II.(1)①“转移”时防止溶液外洒,应将玻璃棒的下端伸入容量瓶的刻度线以下,用玻璃棒引流溶液,故选A;
②FeCl3属于强酸弱碱盐,由于Fe3+的水解使溶液呈酸性,Fe3+水解的离子方程式为Fe3++3H2O![]() Fe(OH)3+3H+,因此,本题答案为:Fe3+ + 3H2O
Fe(OH)3+3H+,因此,本题答案为:Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+;
Fe(OH)3 + 3H+;
(2)根据资料,红棕色溶液中含[Fe(HSO3)]2+,该过程中元素的化合价没有变化,反应的化学方程式为SO2+FeCl3+H2O![]() [Fe(HSO3)]Cl2+2HCl,因此,本题答案为:FeCl3+ SO2 + H2O
[Fe(HSO3)]Cl2+2HCl,因此,本题答案为:FeCl3+ SO2 + H2O ![]() [Fe(HSO3)]Cl2 + HCl;
[Fe(HSO3)]Cl2 + HCl;
(3)出现红棕色是发生了反应SO2+FeCl3+H2O![]() [Fe(HSO3)]Cl2+2HCl,缩短红棕色时间,使上述平衡向逆反应方向移动。因此,本题答案为:增大H+浓度,使“ FeCl3+ SO2 + H2O
[Fe(HSO3)]Cl2+2HCl,缩短红棕色时间,使上述平衡向逆反应方向移动。因此,本题答案为:增大H+浓度,使“ FeCl3+ SO2 + H2O ![]() [Fe(HSO3)]Cl2 + HCl”平衡逆向移动,加快预期反应的速率;
[Fe(HSO3)]Cl2 + HCl”平衡逆向移动,加快预期反应的速率;


科目:高中化学 来源: 题型:
【题目】为倡导“节能减排”和“低碳经济”,目前工业上有一种方法是用CO2来生产燃料乙醇。一定条件下发生反应:2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) ΔH<0。
CH3CH2OH(g)+3H2O(g) ΔH<0。
(1)在一定条件下,在20 L密闭容器中按物质的量比为1∶3充入CO2和H2,温度在450 K,n(H2)随时间变化如表所示:
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 6 | 5 | 5 |
在450 ℃、0~1 min,v(CH3CH2OH)=________;此温度下该反应的化学平衡常数为________(结果保留三位有效数字)。
(2)在5 MPa下测得平衡体系中各物质的体积分数随温度的变化曲线如图所示:

曲线乙表示的是 ________(填物质的化学式)的体积分数,图像中A点对应的体积分数b=________%(结果保留三位有效数字)。
(3)下列措施中能使化学平衡向正反应方向移动的是________。
A.升高温度
B.将CH3CH2OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l mol CO2和3 mol H2
(4)25 ℃、1.01×105Pa时,9.2 g液态乙醇完全燃烧,当恢复到原状态时,放出273.4 kJ的热量,写出表示乙醇燃烧的热化学方程式:________________________。
(5)以石墨为电极,氢氧化钠、乙醇、水、氧气为原料,可以制成乙醇的燃料电池,写出发生还原反应的电极反应式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g),下列可以判断该分解反应已经达到化学平衡状态的是( )
2NH3(g)+CO2(g),下列可以判断该分解反应已经达到化学平衡状态的是( )
A. 2v(NH3)=v(CO2) B. 密闭容器中总压强不变
C. 密闭容器中混合气体的平均摩尔质量不变 D. 密闭容器中氨气的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) △H=xkJ·mol-l
已知:①C(s)+O2(g)=CO2(g) △H=akJ·mol-l
②K2S(s)=S(s)+2K(s) △H=bkJ·mol-l
③2K(s)+N2(g)+3O2(g)=2KNO3(s) △H=ckJ·mol-l
下列说法正确的是
A. x>0 a<0
B. b<0 c<0
C. x=3a-b-c
D. 1mol 碳(s)在空气中不完全燃烧生成CO的焓变小于akJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
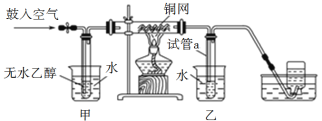
(1)实验过程中铜网出现红色和黑色交替的现象,实际上是发生了两个化学反应,请写出它们的化学方程式_______、______。
(2)甲和乙两个水浴作用不相同。甲的作用是________________,乙的作用是________________。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是_______;集气瓶中收集到的气体的主要成分是_______________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有________________。要除去该物质,可先在混合液中加入________(填字母),然后再通过蒸馏即可除去。
a 氯化钠溶液 b 苯 c 碳酸氢钠溶液 d 四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
①1 L 0.1 mol·![]() NH4Cl溶液中,
NH4Cl溶液中,![]() 的数量为0.1 NA
的数量为0.1 NA
②0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2 NA
③标准状况下,22.4 L二氯甲烷的共价键数为7NA个
④一定条件下,2 mol SO2和1 mol O2混合在密闭容器中充分反应后容器中的分子数大于2 NA
⑤31g白磷P4中含P—P单键数目为6NA
⑥2 mL 0.5 mol/L FeCl3溶液滴入沸水中制备Fe(OH)3胶体,所得胶粒数目小于0.001 NA
A. ①④⑥ B. ②④⑥ C. ②④⑤ D. ②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g) + I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
A. 反应物的总能量高于生成物的总能量
B. 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
C. 断开2 mol H-I键所需能量约为(c+b+a) kJ
D. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用所学知识,解决下列问题:
(1)AgNO3的水溶液呈______(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_____;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,目的是______。
(2)今有常温下五种溶液:NH4Cl溶液 CH3COONa溶液 (NH4)2SO4溶液 NH4HSO4溶液 NaOH溶液
①NH4Cl溶液的pH_____7(填“>”、“<”或“=”),升高温度可以_______(填“促进”或“抑制”)NH4Cl的水解;
②pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH_______NaOH溶液的pH(填“>”“=”或“<”);
③浓度相同的下列三种溶液:(A)NH4Cl溶液(B) (NH4)2SO4溶液(C)NH4HSO4 溶液,则c(NH4+)由大到小的顺序为____>___>____(用序号填空)。
(3)蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合并加热,可得到无水AlCl3,试解释原因________。 (提示:SOCl2与水反应的化学方程式为SOCl2 +H2O= SO2↑+ 2HCl↑)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关容量瓶的四种说法,正确的一组是
①标有使用温度、容积和一条刻度线;
②不宜贮存溶液;
③不能用来加热,不能作反应器;
④使用之前要检查是否漏水;
⑤容量瓶用蒸馏水洗净后,应干燥后再配制溶液。
A. 仅①②③④ B. 仅②③ C. 仅①②④⑤ D. 仅②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com