
| A.2∶3 | B.3∶2 | C.1∶2 | D.1∶1 |
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源:不详 题型:填空题
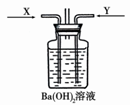
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
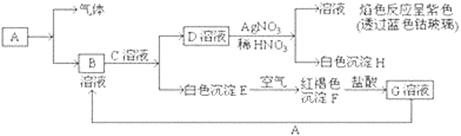
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
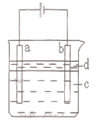
| A.a电极发生的电极反应:4OH--4e-=O2↑+2H2O |
| B.为了在较短时间内看到白色沉淀,可适当加大电压 |
| C.c可以是氯化钠溶液,d可以是苯 |
| D.为了在较短时间内看到白色沉淀,可以剧烈地搅拌溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯水和氯化亚铁溶液 | B.铁屑和氯化铜溶液 |
| C.铁屑和过量稀硫酸 | D.过量铁屑和氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.韧性比生铁好 | B.在冷的浓硫酸中钝化 |
| C.不能与盐酸反应 | D.在冷的浓硝酸中钝化泛使用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
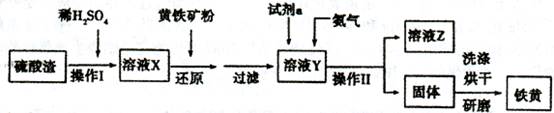
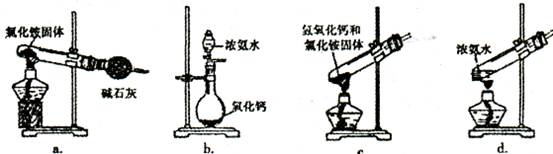
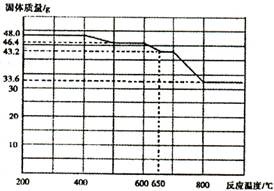
| 加入试剂 | 现象 | 结论 |
| | | 则还原产物为 |
| | | |
| | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁恰好将Fe3+全部还原 |
| B.往反应后溶液中滴入KSCN溶液,不显红色 |
| C.溶液变为浅绿色 |
| D.Fe2+和Fe3+物质的量之比为6:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com