
【题目】如图是利用试纸、铅笔芯设计的微型实验.以铅笔芯为电极,分别接触表面皿上的试纸,接通电源,观察实验现象.下列说法错误的是( )
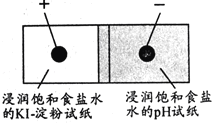
A.pH试纸变蓝
B.KI﹣淀粉试纸变蓝
C.通电时,电能转换为化学能
D.电子通过pH试纸到达KI﹣淀粉试纸
科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(s)cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )
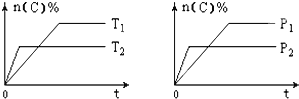
A. 根据图象无法确定改变温度后平衡移动方向
B. 使用催化剂,C的物质的量分数增加
C. 化学方程式系数a>c+d
D. 升高温度,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物在生产生活中有广泛应用,其吸收处理也十分重要。
(1)完成并配平下列离子方程式_____。
Fe3++ SO2+ → Fe2++ SO42-+
(2)标明电子转移的方向和数目______: Fe3++ SO2……。
(3)在Na2SO3溶液中滴加酚酞,溶液呈红色,若在该溶液中滴入过量的BaCl2溶液,实验现象为:_____。请结合离子方程式,运用平衡原理进行解释_____。
(4)在NaClO溶液中通入SO2,写出反应的离子方程式:_____。
(5)在0.1mol/LNa2SO3溶液中,下列关系式正确的是_____。
a.[Na+]+[H+]=[SO32-]+[HSO3-]+[OH-] b.[Na+]>[SO32-]>[OH-]>[H+]
c.[Na+]=2[SO32-]+2[HSO3-]+2[H2SO3] d.[Na+]=2[SO32-]>[OH-]=[H+]
(6)向该溶液中加入少量Na2SO3固体,![]() ___(填“增大”“减小”或“不变”)。
___(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有SiO32—、OH—、CO32—、SO42—、AlO2—、HCO3—、Na+、Mg2+、Fe3+、Al3+ 等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是

A.原溶液中一定含有Na2SO4
B.反应最后形成的溶液中的溶质只有NaCl
C.原溶液中含有CO32- 与AlO2- 的物质的量之比为1∶2
D.原溶液中一定含有的阴离子是:OH—、CO32—、SiO32—、AlO2—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性氧化锌是一种多功能性的新型无机材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:

已知各相关氢氧化物沉淀pH范围如下表所示:
Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
完成下列填空
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯外,还需要_______(选填编号)
A.电子天平 B.量筒 C.容量瓶 D.胶头滴管
(2)步骤II中通过加入KMnO4氧化,并用ZnO调节pH,可以除去含铁杂质.检验沉淀是否完全的实验操作是_________.调节pH的适宜范围是_________.
(3)步骤III中加入Zn粉的作用是:①________;②进一步调节溶液pH.
(4)步骤IV中使用热NH4HCO3溶液能促进Zn2+转化为沉淀,但温度不宜过高,其原因可能是________.
(5)步骤V在_______(填仪器名称)中进行,已知碱式碳酸锌的化学式为Zn5(OH)6(CO3)2,请写出发生反应的化学方程式:________.判断已分解完全的操作是________.
(6)用如下方法测定所得活性氧化锌的纯度:
①取1.000g活性氧化锌,用15.00mL 1.000mol/L硫酸溶液完全溶解
②用浓度为0.500mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL.
假设杂质不参与反应,则所得活性氧化锌的纯度为_______.若在滴定时,实际操作中过量半滴(1mL溶液为25滴),则本次滴定的相对误差为_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行下列实验:

下列说法正确的是( )
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 乙针筒里的现象 |
A | H2S | CuSO4溶液 | 产生黑色沉淀 |
B | H2S | FeSO4溶液 | 产生黑色沉淀 |
C | SO2 | H2S | 出现淡黄色固体 |
D | SO2 | 紫色石蕊溶液 | 先变红后褪色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应对应的离子方程式正确的是( )
A.次氯酸钠溶液中通入过量二氧化硫ClO﹣+H2O+SO2→HClO+HSO3﹣
B.向碳酸氢钠溶液中加入过量氢氧化钙溶液2HCO3﹣+Ca2++2OH﹣→CaCO3↓+2H2O+CO32-
C.氢氧化钡溶液与硫酸溶液反应得到中性溶液Ba2++OH﹣+H++SO42﹣→BaSO4↓+H2O
D.50 mL 1mol/L的NaOH溶液中通入0.03mol H2S:5OH﹣+3H2S→HS﹣+2S2﹣+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时几种物质的溶解度见下表。室温下,向500g硝酸钾饱和溶液中投入2g食盐,下列推断正确的是( )
物质 | 溶解度( g/100g水) |
氯化钠 | 36 |
硝酸钾 | 32 |
硝酸钠 | 87 |
氯化钾 | 37 |
A.食盐不溶解
B.食盐溶解,无晶体析出
C.食盐溶解,析出2 g硝酸钾晶体
D.食盐溶解,析出2 g氯化钾晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C12H14O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:
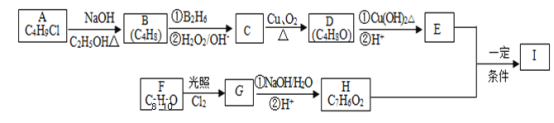
已知以下信息:
①A的核磁共振氢谱表明其只有一种化学环境的氢;
②R-CH=CH2 ![]() R-CH2-CH2-OH;
R-CH2-CH2-OH;
③化合物F苯环上的一氯代物只有两种且遇Fe3+不变色;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A的结构简式为_____,C的名称为________;
(2)B所含官能团的名称是_______,E的分子式为________;
(3)A→B、C→D的反应类型分别为________、________。
(4)写出F→G的化学方程式:___________;
(5)I的结构简式为___________;
(6)I的同系物J比I相对分子质量小28,J的同分异构体中能同时满足如下条件:①苯环上只有一个取代基;②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有____种(不考虑立体异构)。上述同分异构体中有一种发生银镜反应并酸化后核磁共振氢谱为五组峰,且峰面积比为1:2:2:2:3,写出J的这种同分异构体的结构简式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com