
【题目】二茂铁可用作燃料的节能消烟剂、抗爆剂等。实验室制备二茂铁装置示意图如右下图(二茂铁熔点是173℃,在100℃时开始升华;沸点是249℃)。实验步骤为:
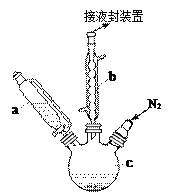

①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a中加入60mL无水乙醚到烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a滴入5.5mL新蒸馏的环戊二烯(密度0.95g/cm3),搅拌;
③将6.5g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25ml装入仪器a中,慢慢滴入仪器c中,45min滴完,继续搅拌45min;
④再从仪器a加入25mL无水乙醚搅拌;
⑤将c中的液体转入仪器d,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的名称是_________,作用是_________________________。
(2)步骤①中通入氮气的目的是________________________________。
(3)仪器c的适宜容积应为______:①100ml、②250ml、③500ml;仪器a使用前应进行的操作是_____,其操作过程为:关闭恒压滴液漏斗颈部旋塞_______________________。
(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为________________________________;步骤⑦是二茂铁粗产品的提纯,该过程在右图中进行,其操作名称为__________。
(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是_____。
(6)最终得到纯净的二茂铁3.7g,则该实验的产率为_______(保留两位有效数字)。
【答案】 球形冷凝管 冷凝回流有机物(或乙醚、环戊二烯和二甲亚砜) 将装置中的空气排尽(或排尽、除去氧气),防止(避免、不让)实验过程中Fe2+被氧化 ② 检漏或检查是否漏水 从上口加入适量的蒸馏水,观察旋塞是否漏水;若不漏水,关闭上口旋塞,倒立检查是否漏水,正立、再将上口旋塞旋转180度,再倒立检查是否漏水 2KOH+FeCl2+2C5H6=== Fe(C5H5)2+2KCl+2H2O 升华 测定所得固体的熔点 50%
【解析】(1)仪器b的名称是球形冷凝管,作用是冷凝回流有机物(或乙醚、环戊二烯和二甲亚砜);(2)二茂铁中铁是+2价,易被空气中氧气氧化,步骤①中通入氮气的目的是:通入氮气排尽装置中空气,防止实验过程中亚铁离子被氧化。(3)仪器c为三颈烧瓶,由题意可知共加入液体110mL,三颈烧瓶中盛放液体的体积不超过容积的2/3,所以选择250ml;仪器c的适宜容积应为②250ml;分液漏斗使用前应进行的操作是:检漏或检查是否漏水,其操作过程为:关闭恒压滴液漏斗颈部旋塞从上口加入适量的蒸馏水,观察旋塞是否漏水;若不漏水,关闭上口旋塞,倒立检查是否漏水,正立、再将上口旋塞旋转180度,再倒立检查是否漏水。(4)KOH、FeCl2、C5H6反应生成二茂铁[Fe(C5H5)2]和KCl的化学方程式为 2KOH+FeCl2+2C5H6=== Fe(C5H5)2+2KCl+2H2O;步骤⑦是二茂铁粗产品的提纯,二茂铁有固体直接变成气体,然后冷凝收集,其操作名称为升华;(5)为了确证得到的是二茂铁,还需要进行的一项简单实验是测定所得固体的熔点。(6)二茂铁的理论产量为![]() ×
×![]() ×186g·mol-1=7.4g,则产率=3.7g/7.4g×100%=50%;
×186g·mol-1=7.4g,则产率=3.7g/7.4g×100%=50%;


科目:高中化学 来源: 题型:
【题目】三蝶烯是最初的“分子马达”的关键组件,三碟烯某衍生物X可用于制备吸附材料,其结构如图所示,3个苯环在空间上互为120°夹角。下列有关X的说法错误的是

A. 分子式为C22H14O4
B. 能发生加成、取代反应
C. 苯环上的一氯代物有3种
D. 分子中最多可能有20个原子位于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机反应中间体(M)的一种合成路线如下图所示。
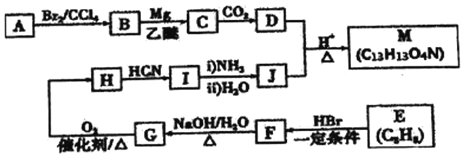
已知:①![]()
②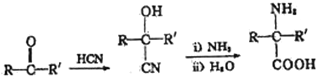 (R表示氢原子或烃基)
(R表示氢原子或烃基)
③标准状况下,气态烃A 的密度是H2的14倍。
④芳香族化合物H能发生银镜反应。
⑤M 中还有一个除苯环之外的环状结构。
(1)B的名称(系统命名)为________;H→I的反应类型为_________。
(2) E 中官能团的结构简式为_________。
(3)F→G 的化学方程式为_________。
(4)D+J→M的化学方程式为__________。
(5) 写出符合下列条件的J的所有同分异构体的结构简式:_________ (不考虑立体异构)。
①苯环上连有-NO2 ②核磁共振氢谱有3个峰
(6) 结合已有知识和相关信息。写出以CH3CHO和题中的物质为原料制备分子式为C6H10N2O2(含六元环)的物质的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:_____________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是( )
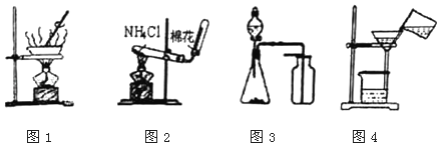
A. 用图1所示装置进行食盐溶液的蒸发结晶 B. 用图2所示装置在实验室制取少量氨气
C. 用图3所示装置制取少量CO2、O2或NO D. 用图4所示装置进行固液物质的分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.均一稳定的分散系只有溶液
B.胶体和溶液、浊液的本质区别是能否产生“丁达尔效应”
C.一束平行光线照射FeCl3溶液时,从垂直于光线的方向可以看到一条光亮的通路
D.氢氧化铁胶体能吸附水中的悬浮颗粒并沉降,起到净水作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷在氧气中燃烧,可能生成两种固态氧化物.3.1g的单质磷(P)在3.2g的氧气中燃烧,至反应物耗尽,并放出XKJ热量。
(1)通过计算确定反应产物的组成(用化学式表示)是________。
(2)已知单质磷的燃烧热为Y KJ/mol,则1mol P与O2反应生成固态P2O3的热化学反应方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用0.2mol·L-1 HA溶液与0.2mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则
(1)该溶液显_____性(填“酸”、“碱”或“中”),原因是______________(用离子方程式表示)
(2)混合溶液中c(HA)+c(A-)____0.1mol·L-1(填“>”、“<”或“=”,下 同)
(3)如果取0.2mol·L-1HA溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度____NaA的水解程度。
(4)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA- HA-![]() H++A2-
H++A2-
回答下列问题:
①Na2A溶液显____________(填“酸性”,“中性”,或“碱性”)。理由是____________________________________________(用离子方程式表示)
②在0.1mol·L-1的Na2A溶液中,下列微粒浓度关系式正确的是__________
A.c(A2-)+c(HA-)+c(H2A)=0.1mol·L-1
B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金.请回答:(题目中的百分含量均为质量分数)

(1)钢是含碳量为0.03%~2%的________(填物质类别名称).
(2)如图所示的装置中,甲、乙、丙三个烧杯分别盛放足量的溶液,电极及溶液如下表所示:
电极 | a | b | c | d | e | f |
石墨 | 石墨 | 铜 | 钢 | 钢 | 铜 | |
溶液 | NaCl溶液 | CuSO4溶液 | CuSO4溶液 | |||
通电后电极a上可产生能使湿润的碘化钾淀粉试纸变蓝的气体.
①上述装置中M极为直流电源的________极(填“正”或“负”),电极b上发生的电极反应式为________.
②若在钢币上镀铜,应选择_________烧杯(填“乙”或“丙”),当电极a上生成标准状况下气体2240mL时,理论上可在电极________(填字母)上镀铜________g.
(3)工业上以铝土矿(主要成分Al2O3nH2O,含少量的氧化铁和石英等杂质)为原料生产铝.为除去铝土矿样品中氧化铁和石英杂质,要将粉碎、筛选后的铝土矿样品溶解在足量的氢氧化钠溶液中处理,请写出有关反应的离子方程式 ________.
(4)已知硬铝中含Cu:2.2%~5%、Mg:0.2%~3%、Mn:0.3%~1.5%、Si:0.5%,其余是Al.1角硬币单枚质量为2.20克,若想制得1角硬币1百万枚,理论上至少需要含Al2O3 90%的铝土矿约________吨(小数点后保留一位数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
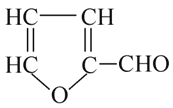
【题目】玉米芯与稀硫酸在加热加压下反应,可以制得糠醛(结构简式如图)。 糠醛是重要的化工原料,用途广泛。 关于糠醛的说法,不正确的是
A. 糠醛能使酸性高锰酸钾溶液褪色
B. 1mol糠醛可与2mo lH2 发生加成反应
C. 其核磁共振氢谱有4种不同类型的吸收峰
D. 加热时糠醛与新制的 Cu(OH)2 悬浊液反应生成红色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com