
ΓΨΧβΡΩΓΩΡ≥Έό…ΪΙΛ“ΒΖœΥ°÷–Ω…ΡήΚ§”–Na+ΓΔMg2+ΓΔAl3+ΓΔCu2+ΓΔCl-ΓΔSO42-÷–ΒΡΦΗ÷÷άκΉ”ΓΘ
aΘ°»Γ10 mLΗΟΖœΥ°”Ύ ‘Ιή÷–Θ§Φ”»κΉψΝΩΒΡBa(NO3)2»ή“ΚΚΆœΓœθΥαΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§≥δΖ÷Ζ¥”ΠΚσΙΐ¬ΥΘ§œρ¬Υ“Κ÷–Φ”»κAgNO3»ή“ΚΈό≥ΝΒμ≤ζ…ζΓΘ
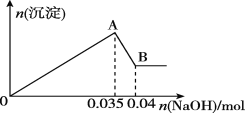
bΘ°Νμ»Γ10 mLΗΟΖœΥ°”Ύ ‘Ιή÷–Θ§ΒΈΦ”NaOH»ή“Κœ»≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§Κσ≤ΩΖ÷≥ΝΒμ»ήΫβΘ§…ζ≥…≥ΝΒμΒΡΈο÷ ΒΡΝΩΥφΦ”»κNaOHΒΡΈο÷ ΒΡΝΩΙΊœΒ»γΆΦΥυ ΨΓΘ
ΗυΨί…œ ω Β―ιΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©ΗΟΖœΥ°÷–“ΜΕ®≤ΜΚ§”–ΒΡάκΉ””–______________(ΧνάκΉ”ΖϊΚ≈)
Θ®2Θ© Β―ι “≈δ÷Τ100 mL 1.0 molΓΛL-1ΒΡNaOH»ή“Κ ±Θ§”ΟΒΫΒΡ≤ΘΝß“«Τς≥ΐ…’±≠ΓΔ≤ΘΝßΑτΓΔΝΩΆ≤ΆβΘ§ΜΙ–η“Σ______________(Χν“«ΤςΟϊ≥Τ)
Θ®3Θ©–¥≥ωAΓζBΙΐ≥Χ÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ______________
Θ®4Θ©ΗΟΖœΥ°÷–Θ§c(Al3+)=____________
ΓΨ¥πΑΗΓΩCu2ΘΪΓΔClΘ≠100 mL»ίΝΩΤΩΓΔΫΚΆΖΒΈΙήAl(OH)3ΘΪOHΘ≠=AlO2Θ≠ΘΪ2H2O0.5 molΓΛLΘ≠1
ΓΨΫβΈωΓΩ
Έό…Ϊ»ή“Κ÷–≤ΜΜα¥φ‘Ύ”–…ΪΒΡCu2+ΘΜa.»Γ10mLΗΟΖœΥ°”Ύ ‘Ιή÷–Θ§Φ”»κΉψΝΩΒΡBa(NO3)2»ή“ΚΚΆœΓœθΥαΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΗΟ≥ΝΒμΈΣΝρΥα±ΒΘ§‘ρ‘≠»ή“Κ÷–Κ§”–SO42-Θ§≥δΖ÷Ζ¥”ΠΚσΙΐ¬ΥΘ§œρ¬Υ“Κ÷–Φ”»κAgNO3»ή“ΚΈό≥ΝΒμ≤ζ…ζΘ§ΥΒΟς‘≠»ή“Κ÷–≤Μ¥φ‘ΎCl-ΘΜb.Νμ»Γ10mLΗΟΖœΥ°”Ύ ‘Ιή÷–Θ§ΒΈΦ”NaOH»ή“Κœ»≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§Κσ≤ΩΖ÷≥ΝΒμ»ήΫβΘ§»ήΫβΒΡ≥ΝΒμΈΣ«β―θΜ·¬ΝΘ§≤Μ»ήΒΡ≥ΝΒμΈΣ«β―θΜ·ΟΨΘ§‘ρ‘≠»ή“Κ÷–“ΜΕ®Κ§”–Mg2+ΓΔAl3+Θ§ΗυΨίΆΦ÷– ΐΨίΦ¥Ω…ΦΤΥψAl3+ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΓΘ
(1).ΗυΨί…œ ωΖ÷ΈωΩ…÷ΣΘ§ΗΟΖœΥ°÷–“ΜΕ®≤ΜΚ§”–ΒΡάκΉ”ΈΣCu2+ΓΔClΘ§Ι ¥πΑΗΈΣΘΚCu2+ΓΔClΘΜ
(2). Β―ι “≈δ÷Τ100mL 1.0molL1ΒΡNaOH»ή“Κ ±Θ§”ΟΒΫΒΡ≤ΘΝß“«Τς≥ΐ…’±≠ΓΔ≤ΘΝßΑτΓΔΝΩΆ≤ΆβΘ§ΜΙ–η―Γ”ΟΙφΗώΈΣ100mLΒΡ»ίΝΩΤΩΘ§Ε®»ί ±±Ί–κ Ι”ΟΫΚΆΖΒΈΙήΘ§Ι ¥πΑΗΈΣΘΚ100mL»ίΝΩΤΩΓΔΫΚΆΖΒΈΙήΘΜ
(3).AΓζBΒΡΙΐ≥ΧΖΔ…ζΒΡΖ¥”ΠΈΣ«β―θΜ·¬Ν”κ«β―θΜ·ΡΤΖ¥”Π…ζ≥…ΤΪ¬ΝΥαΡΤΚΆΥ°Θ§άκΉ”ΖΫ≥Χ ΫΈΣΘΚAl(OH)3+OH=AlO2+2H2OΘ§Ι ¥πΑΗΈΣΘΚAl(OH)3+OH=AlO2+2H2OΘΜ
(4).ΗυΨίΖΫ≥Χ ΫAl(OH)3+OH=AlO2+2H2OΩ…÷ΣΘ§n[Al(OH)3]=n(NaOH)=0.04molΘ≠0.035mol=0.005molΘ§ΗυΨί‘ΣΥΊ ΊΚψΩ…÷Σ‘≠»ή“Κ÷–¬ΝάκΉ”ΒΡΈο÷ ΒΡΝΩΈΣ0.005molΘ§‘ρ‘≠»ή“Κ÷–¬ΝάκΉ”ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣΘΚc(Al3+)=0.005molΓ¬0.01L=0.5mol/LΘ§Ι ¥πΑΗΈΣΘΚ0.5mol/LΓΘ


 Οϊ–ΘΩΈΧΟœΒΝ–¥πΑΗ
Οϊ–ΘΩΈΧΟœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–”–ΙΊΒγ≥ΊΒΡΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A. ÷Μζ…œ”ΟΒΡο°άκΉ”Βγ≥Ί τ”ΎΕΰ¥ΈΒγ≥Ί
B. »Φ…’÷≤ΈοΒΡΫ’Η―ΚΆ÷Π“Ε“‘Μώ»Γ»»ΝΩΚΆΖ Νœ τ”Ύ…ζΈο÷ ΡήΒΡάϊ”ΟΖΫ Ϋ
C. Υυ”–ΒΡ―θΜ·ΜΙ‘≠Ζ¥”ΠΕΦΩ…“‘…ηΦΤ≥…‘≠Βγ≥Ί
D. «β―θ»ΦΝœΒγ≥Ί «“Μ÷÷≤Μ–η“ΣΫΪΜΙ‘≠ΦΝΚΆ―θΜ·ΦΝ»Ϊ≤Ω¥Δ¥φ‘ΎΒγ≥ΊΡΎΒΡ–¬–ΆΖΔΒγΉΑ÷Ο
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈ“Ιζάϊ”ΟΚœ≥…Τχ÷±Ϋ”÷Τœ©ΧΰΜώ÷Ί¥σΆΜΤΤΘ§Τδ‘≠άμ «
Ζ¥”ΠΔΌΘΚC(s)ΘΪ1/2O2(g)=CO(g) ΠΛH1
Ζ¥”ΠΔΎΘΚC(s)ΘΪH2O(g)=CO(g)ΘΪH2(g) ΠΛH2
Ζ¥”ΠΔέΘΚCO(g)ΘΪ2H2(g)=CH3OH(g) ΠΛH3ΘΫΘ≠90.1 kJΓΛmolΘ≠1
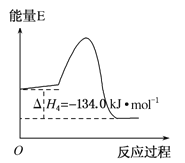
Ζ¥”ΠΔήΘΚ2CH3OH(g)ΓζCH3OCH3(g)ΘΪH2O(g) ΠΛH4Θ§ΡήΝΩ±δΜ·»γΆΦΥυ Ψ
Ζ¥”ΠΔίΘΚ3CH3OH(g)ΓζCH3CH=CH2(g)ΘΪ3H2O(g) ΠΛH5ΘΫΘ≠31.0 kJΓΛmolΘ≠1
œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «( )
A. Ζ¥”ΠΔέ Ι”Ο¥ΏΜ·ΦΝΘ§ΠΛH3Φθ–Γ B. ΠΛH1Θ≠ΠΛH2<0
C. Ζ¥”ΠΔή÷–’ΐΖ¥”ΠΒΡΜνΜ·Ρή¥σ”ΎΡφΖ¥”ΠΒΡΜνΜ·Ρή D. 3CO(g)ΘΪ6H2(g)ΓζCH3CH=CH2(g)ΘΪ3H2O(g) ΠΛHΘΫΘ≠121.1 kJΓΛmolΘ≠1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦν–‘«Ω»θΫι”ΎKOHΚΆMg(OH)2÷°ΦδΒΡ«β―θΜ·Έο «Θ® Θ©
A. NaOH B. Al(OH)3 C. LiOH D. RbOH
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘ΎΈό…Ϊ»ή“Κ÷–Θ§œ¬Ν–άκΉ”Ρή¥σΝΩΙ≤¥φΒΡ «Θ® Θ©
A.Mg2ΘΪΓΔSO42Θ≠ΓΔK ΘΪΓΔClΘ≠B.NaΘΪ ΓΔNH4ΘΪ ΓΔNO3Θ≠ΓΔMnO4Θ≠
C.K ΘΪ ΓΔCu2ΘΪ ΓΔClΘ≠ΓΔBrΘ≠D.Ba2ΘΪ ΓΔNaΘΪ ΓΔNO3Θ≠ΓΔCO32Θ≠
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ“ΜΕ®Έ¬Ε»ΚΆ―Ι«Ωœ¬Θ§Α―ΉΑ”–NOΚΆNO2ΒΡΜλΚœΤχΧεΒΡ ‘ΙήΒΙΝΔ”ΎΥ°÷–Θ§≥δΖ÷Ζ¥”ΠΚσΘ§ ‘ΙήΡΎΤχΧεΒΡΧεΜΐΥθ–ΓΈΣ‘≠ΤχΧεΧεΜΐΒΡ![]() Θ§‘ρ‘≠ΜλΚœΤχΧε÷–NOΚΆNO2ΒΡΧεΜΐ±»ΈΣ(ΓΓΓΓ)
Θ§‘ρ‘≠ΜλΚœΤχΧε÷–NOΚΆNO2ΒΡΧεΜΐ±»ΈΣ(ΓΓΓΓ)
A. 3ΓΟlB. 1ΓΟ3C. 2ΓΟ3D. 3ΓΟ2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»Γ“ΜΕ®ΝΩΒΡFeΓΔCuΒΡΜλΚœΈοΖέΡ©Θ§ΤΫΨυΖ÷≥…AΓΔBΓΔCΓΔDΓΔEΈεΒ»ΖίΘ§Ζ÷±πœρΟΩ“ΜΖί÷–Φ”»κ“ΜΕ®ΝΩΒΡœΓœθΥαΘ§ Β―ι÷– ’Φ·ΒΫΒΡNOΤχΧε(Έ©“ΜΜΙ‘≠≤ζΈο)ΒΡΧεΜΐΦΑΥυΒΟ Θ”ύΈοΒΡ÷ ΝΩΦ«¬Φ»γœ¬(Υυ”–ΧεΜΐΨυ‘Ύ±ξΉΦΉ¥Ωωœ¬≤βΕ®)ΘΚ
Β―ι–ρΚ≈ | A | B | C | D | E |
œθΥα»ή“ΚΧεΜΐ | 100ml | 200 mL | 300 mL | 400 mL | 500 mL |
Θ”ύΙΧΧεΒΡ÷ ΝΩ | 17.2 g | 8g | 0 g | 0 g | 0 g |
ΤχΧεΧεΜΐ | 2.24 L | 4.48 L | 6.72L | 7.84 L | 7.84 L |
Θ®1Θ©AΉι Β―ιΚσ17.2 g Θ”ύΙΧΧεΈΣ________Θ§BΉι Β―ιΚσ8 g Θ”ύΙΧΧεΈΣ_______ΓΘ(ΨυΧν–¥Μ·―ß Ϋ)
Θ®2Θ© Β―ι÷–ΟΩ¥ΈΥυ»ΓΜλΚœΈο÷–ΧζΒΡΈο÷ ΒΡΝΩΈΣ________molΓΘ
Θ®3Θ©»τCΉιΫπ τ«ΓΚΟΖ¥”ΠΆξΘ§‘ρΖ¥”ΠΚσ»ή“Κ÷–ΒΡΫπ τ―τάκΉ”ΈΣΘΚ_____________ Θ§Έο÷ ΒΡΝΩ÷°±» «:________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ¬»‘Ύ“ϊ”ΟΥ°¥Πάμ÷–≥Θ”ΟΉς…±ΨζΦΝΘ§«“HClOΒΡ…±ΨζΡήΝΠ±»ClOΘ≠«ΩΓΘ25Γφ ±¬»Τχ-¬»Υ°ΧεœΒ÷–¥φ‘Ύ“‘œ¬ΤΫΚβΙΊœΒΘΚ
Cl2(g)![]() Cl2(aq) K1=10Θ≠1.2
Cl2(aq) K1=10Θ≠1.2
Cl2(aq)+ H2O![]() HClO + H++ClΘ≠K2=10Θ≠3.4
HClO + H++ClΘ≠K2=10Θ≠3.4
HClO![]() H++ ClOΘ≠Ka=?
H++ ClOΘ≠Ka=?
Τδ÷–Cl2(aq)ΓΔHClOΚΆClOΘ≠Ζ÷±π‘Ύ»ΐ’Ώ÷–Υυ’ΦΖ÷ ΐ(ΠΝ)ΥφpH±δΜ·ΒΡΙΊœΒ»γΆΦΥυ ΨΓΘœ¬Ν–±μ ω’ΐ»ΖΒΡ «Θ® Θ©

A. Cl2(g)+ H2O![]() 2H++ ClOΘ≠+ ClΘ≠K=10Θ≠10.9
2H++ ClOΘ≠+ ClΘ≠K=10Θ≠10.9
B. ‘Ύ¬»¥ΠάμΥ°ΧεœΒ÷–Θ§c(HClO) + c(ClOΘ≠) =c(H+)Θ≠c(OHΘ≠)
C. ”Ο¬»¥Πάμ“ϊ”ΟΥ° ±Θ§pH=7.5 ±…±Ψζ–ßΙϊ±»pH=6.5 ±ΚΟ
D. ¬»¥Πάμ“ϊ”ΟΥ° ±Θ§‘ΎœΡΦΨΒΡ…±Ψζ–ßΙϊ±»‘ΎΕ§ΦΨ≤ν
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“Μ÷÷Ω…≥δΒγο°-Ω’ΤχΒγ≥Ί»γΆΦΥυ ΨΓΘΒ±Βγ≥ΊΖ≈Βγ ±Θ§O2”κLi+‘ΎΕύΩΉΧΦ≤ΡΝœΒγΦΪ¥Π…ζ≥…Li2O2-xΘ®x=0Μρ1Θ©ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «

A. Ζ≈Βγ ±Θ§ΕύΩΉΧΦ≤ΡΝœΒγΦΪΈΣΗΚΦΪ
B. Ζ≈Βγ ±Θ§ΆβΒγ¬ΖΒγΉ””…ΕύΩΉΧΦ≤ΡΝœΒγΦΪΝςœρο°ΒγΦΪ
C. ≥δΒγ ±Θ§ΒγΫβ÷ »ή“Κ÷–Li+œρΕύΩΉΧΦ≤ΡΝœ«χ«®“Τ
D. ≥δΒγ ±Θ§Βγ≥ΊΉήΖ¥”ΠΈΣLi2O2-x=2Li+Θ®1Θ≠![]() Θ©O2
Θ©O2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com