
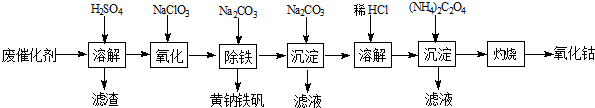

分析 钴废催化剂加入稀硫酸,发生Co+H2SO4=CoSO4+H2↑,Fe+H2SO4=FeSO4+H2↑,过滤滤渣是不溶的二氧化硅,而滤液是硫酸钴、硫酸亚铁与过量的硫酸的混合溶液,向滤液中加氯酸钠将亚铁离子氧化成铁离子,然后加入碳酸钠得到黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,继续向滤液中加入碳酸钠,得到碱式碳酸钴[(CoCO3)2•3Co(OH)2],然后用盐酸溶解碱式碳酸钴[(CoCO3)2•3Co(OH)2],再向所到溶液中加入草酸铵,得到溶解度极小的草酸钴,最后燃烧生成氧化钴;
(1)洗液与滤液合并,提高洗涤和滤液中钴的利用率,滤渣应该是原料中不溶于稀硫酸的成分;
(2)亚铁离子被氯酸根离子氧化成铁离子,根据得失电子守恒分析解答;根据3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色沉淀);4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3↓(蓝色沉淀),如果亚铁离子部分氧化,滴加无色的硫氰化钾生成蓝色沉淀,可向氧化后的溶液中滴入硫氰化钾,观察是否有蓝色沉淀生成;
(3)生成硫酸铁与碳酸钠发生双水解得到黄钠铁矾,书写化学方程式;
(4)沉淀洗涤的方法是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次;
(5)CoCl2的溶解度曲线可知,随温度的升高,CoCl2的溶解度增大,所以趁热过滤,防止温度降低氯化钴析出;
(6)CoC2O4的质量为1.470g,其我知道可为0.01mol,Co元素质量为0.59g,钴氧化物质量为0.83g,氧化物中氧元素质量为0.83g-0.59g=0.24g,则氧化物中Co原子与O原子物质的量之比为0.01mol:$\frac{0.24}{16}$≈2:3,故Co氧化物为Co2O3.
解答 解:(1)洗液与滤液合并,提高洗涤和滤液中钴的利用率,故答案为:提高钴等元素的利用率;
(2)亚铁离子被氯酸根离子氧化成铁离子,1molr的亚铁离子失去1mol的电子,而1mol的氯酸根离子得到6mol的电子,根据电子得失守恒,可知离子方程式为:6Fe2++6H++ClO3-$\frac{\underline{\;加热\;}}{\;}$6Fe3++Cl-+3H2O,取氧化后的溶液少许于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则Fe2+已全部被氧化,故答案为:6Fe2++6H++ClO3-$\frac{\underline{\;加热\;}}{\;}$6Fe3++Cl-+3H2O;取氧化后的溶液少许于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则Fe2+已全部被氧化;
(3)生成硫酸铁与碳酸钠发生双水解得到黄钠铁矾,化学反应方程式为:3Fe2(SO4)3+6H2O+6 Na2CO3=Na2Fe6(SO4)4(OH)12↓+5 Na2SO4+6CO2↑,故答案为:3Fe2(SO4)3+6H2O+6 Na2CO3=Na2Fe6(SO4)4(OH)12↓+5 Na2SO4+6CO2↑;
(4)沉淀洗涤的方法是向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次,
故答案为:向漏斗中加入蒸馏水至浸没沉淀,静置使滤液流出.重复操作2~3次;
(5)CoCl2的溶解度曲线可知,随温度的升高,CoCl2的溶解度增大,所以趁热过滤,防止温度降低氯化钴析出,故答案为:防止因温度降低,CoCl2晶体析出;
(6)CoC2O4的质量为1.470g,其我知道可为0.01mol,Co元素质量为0.59g,钴氧化物质量为0.83g,氧化物中氧元素质量为0.83g-0.59g=0.24g,则氧化物中Co原子与O原子物质的量之比为0.01mol:$\frac{0.24}{16}$≈2:3,故Co氧化物为Co2O3,故答案为:Co2O3.
点评 本题考查化学方程的书写、离子的检验、沉淀的洗涤、对图象的分析处理等,需要学生具备知识的基础,难度中等.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有6.02×1023个Cl2分子 | B. | 气体体积为22.4L | ||
| C. | 含有1.204×1024个Cl原子 | D. | 气体质量为35.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①④⑥ | C. | ③⑤ | D. | ①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数为34、中子数为18的核素:${\;}_{16}^{34}$S | |
| B. | S2-的结构示意图 | |
| C. | CS2的结构式:S-C-S | |
| D. | 亚硫酸的电离方程式:H2SO3?2H++SO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污 | |
| B. | 自来水厂可用明矾对水进行消毒杀菌 | |
| C. | 常温下,浓硝酸不跟铁发生化学反应,可用铁制容器盛装浓硝酸 | |
| D. | MgO、Al2O3熔点高,可用于制作耐火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W<X<Y<Z | |
| B. | X、Y、Z单质的熔点:Z<Y<X | |
| C. | 简单气态氢化物的热稳定性:Y<Z<W | |
| D. | Z元素的最高价氧化物对应水化物的分子中存在非极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温室效应是当今世界面临的环境问题,使温室效应增强的气体只有二氧化碳 | |
| B. | 侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异 | |
| C. | 家庭用的“84”消毒液与洁厕灵不能同时混合使用,否则会发生中毒事故 | |
| D. | 实验室里熔化氢氧化钠时,可选用石英坩埚和铁坩埚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| B. | 金属汞一旦洒落到实验室地面或桌面时,必须尽可能收集,并深埋处理 | |
| C. | 金属钠着火时用泡沫灭火器灭火 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO | |
| B. | 生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应 | |
| C. | 粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法 | |
| D. | 黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com