


科目:高中化学 来源:不详 题型:单选题
| A.a=4b+3c | B.a=4b+c | C.a:b=4:1 | D.a:b=4:3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
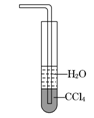
| A.氨气可以用浓硫酸干燥也可用碱石灰干燥 |
| B.氨水能导电,所以NH3是电解质 |
| C.稳定性:NH3<CH4 |
| D.用水吸收NH3用右图装置可防止倒吸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:1:1 | B.2:1:1 | C.3:7:4 | D.1:5:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通常状况下,氨的溶解度不大 | B.氨水中的NH3·H2O电离出少量的OH- |
| C.溶于水的氨分子只有少量电离 | D.氨本身的碱性弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2和H2在点燃或光照条件下合成氨 |
| B.氨的稳定性比磷化氢弱 |
| C.氨极易溶于水,氨水呈碱性,主要含 NH4+和OH- |
| D.由氨制取硝酸铵的过程中,氨表现出还原性和碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有Fe3+ | B.只有Fe2+ | C.有Fe2+和Fe3+ | D.无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com