
| A、滴定时,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时,为滴定终点 |
| B、滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量 |
| C、碱式滴定管若滴定前平视读数、滴定后俯视读数,则测定结果偏高 |
| D、锥形瓶用水洗净后未用食醋润洗,则测得的食醋浓度偏低 |


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
| A、向盐酸中滴加氨水:H++OH-=H2O | ||||
B、氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH-
| ||||
| C、氢氧化镁与稀硫酸反应:H++OH-═H2O | ||||
| D、单质铜与稀硝酸反应:Cu+2H++2NO3-═Cu2++2NO↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S |
| B、S |
| C、FeS |
| D、FeSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
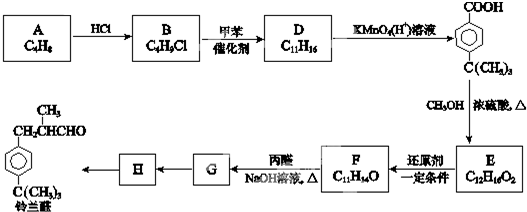
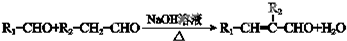
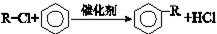
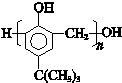 ,合成路线如图2,写出第三步的方程式:
,合成路线如图2,写出第三步的方程式: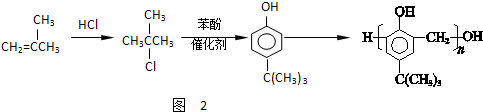
查看答案和解析>>
科目:高中化学 来源: 题型:

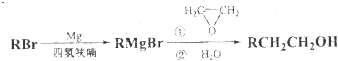
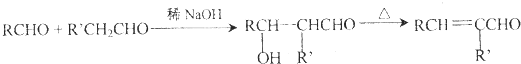
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
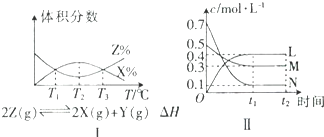
| A、由图Ⅰ可知,该反应在T2时达到平衡 |
| B、由Ⅰ图可知,该反应的△H<0 |
| C、图Ⅱ发生反应的化学方程式为2M+6N?3L |
| D、由图Ⅱ可知,若密闭容器中M、N、L的起始浓度依次为0.4mol/L、0.4mol/L、0.2mol/L,保持其他条件不变,达到平衡时L的浓度为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称取8gNaOH固体,放入100mL量筒,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL |
| B、称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 |
| C、用50mL量筒量取50mL4mol/LNaOH溶液,倒入100mL烧杯中,再用同一量筒取50mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
| D、称取8gNaOH固体放入300mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应是溴乙烷的水解反应 |
| B、往反应后的溶液中直接加入AgNO3溶液检验是否有Br-生成 |
| C、该反应产物中有水、钠盐和不饱和烃 |
| D、生成的气体可直接通入到溴水中检验是否有乙烯生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com