
| A. | 铝粉与Fe2O3高温下反应 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | NaOH与H2SO4的中和反应 | D. | 灼热的炭与CO2反应 |
分析 有元素化合价变化的反应,为氧化还原反应;反应物总能量比生成物能量大,则反应为放热反应,结合常见的放热反应来解答.
解答 解:A.反应生成氧化铝和Fe,Al、Fe元素的化合价变化,属于氧化还原反应,且属于放热反应,故A选;
B.没有元素的化合价变化,不属于氧化还原反应,属于吸热反应,故B不选;
C.中和反应中一定没有元素的化合价变化,不属于氧化还原反应,属于放热反应,故C不选;
D.灼热的炭与CO2反应生成CO,C元素的化合价变化,属于氧化还原反应,但为吸热反应,故D不选;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析能力和氧化还原反应判断、放热反应判断的考查,题目难度不大.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:解答题

| 硫酸% | 31.52 | 36.10 | 40.67 | 45.25 |
| 锰浸出率 | 77.42 | 89.49 | 91.59 | 97.95 |
| 黄铁矿% | 12.5 | 15 | 17.5 | 20 |
| 锰浸出率 | 88.79 | 97.95 | 99.18 | 99.46 |
| A | 硫酸45.25% | B | 硫酸31.52% | C | 硫酸45.25% | D | 硫酸36.10% |
| 黄铁矿20% | 黄铁矿15% | 黄铁矿15% | 黄铁矿20% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:CH4>SiH4 | B. | 碱性:Mg(OH )2>Ca(OH )2 | ||
| C. | 羟基中H的活泼性:H2O>CH3CH2OH | D. | 原子半径:S>Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(N2生成)=3υ(H2消耗) | |
| B. | H2、H2、HN3的分子数之比为1:3:2 | |
| C. | 单位时间内生成2molNH3,同时消耗1molH2 | |
| D. | 容器内的压强不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
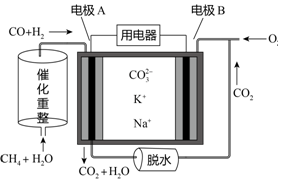
| A. | 电极A上H2和CO都发生了氧化反应 | |
| B. | 反应CH4+H2O$\frac{\underline{\;催化剂\;}}{△}$3H2+CO,每消耗1molCH4转移12mol电子 | |
| C. | 电池工作时,电能转变为化学能 | |
| D. | 电极B上发生的电极反应为:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极附近硫酸根离子浓度增大 | |
| B. | 负极附近硫酸根离子浓度增大 | |
| C. | 正负极附近硫酸根离子浓度基本不变 | |
| D. | 若锌片、铜片同时有气泡冒出时,说明锌做正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com