
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:2016-2017学年广西桂林十八中高二上期中文化学卷(解析版) 题型:选择题
苹果汁是人们喜爱饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色,若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
A.氧化性 B.还原性 C.碱性  D.酸性
D.酸性
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练二化学试卷(解析版) 题型:选择题
在一定温度下,向2 L恒容密闭容器中充入1mol A,发生A(g)  B(g) + C(g)反应。反应过程中c(C)随时间变化的曲线如下图所示,下列说法不正确的是( )
B(g) + C(g)反应。反应过程中c(C)随时间变化的曲线如下图所示,下列说法不正确的是( )
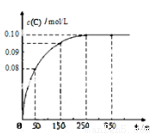
A.反应在 0 ~50 s 的平均速率v(C)=1.6×10-3mo1/(L • s)
B.该温度下,反应的平衡常数值为0.025
C.反应平衡后,再向容器中充入A、B、C各1mol,此时v(正)<v(逆)
D.保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
某化学科研小组研宄在其他条件不变时,改变某一条件对A2(g) +3B2 (g)  AB3 (g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如图可得出的判断结论正确的是
AB3 (g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如图可得出的判断结论正确的是

A.反应速率a>b>c
B.若T2>T1,则正反应一定是吸热反应
C.达到平衡时,AB3的物质的量大小为:b>c>a
D.达到平衡时A2的转化率大小为:b>a>c
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列有关化学研究的正确说法是
A. 同时改变两个变量来研究反应速率的变化,能更快得出有关规律
B. 对于同一个化学反应,无论是正反应还是逆反应,其反应的焓变相同
C. 根据11~17号元素最高价氧化物对应水化物的酸碱性递变规律,推出同周期元素的金属性、非金属性递变规律
D. 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列描述的元素中,一定属于主族元素的有
A. 元素的原子最外层电子个数为2
B. 元素的原子最外层电子个数为6
C. 位于元素周期表中ⅡA族右边的元素
D. 阴离子RO4﹣中R元素
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:填空题
(1)实验测得,4g甲醇液态在氧气中充分燃烧生成二氧化碳气体和液态水时释放出90kJ的热量,试写出甲醇燃烧的热化学方程式:_________________。
(2) 已知反应N2(g)+3H2(g) 2NH3(g) △H=a kJ/mol。试根据表中所列键能数据估算a的数值:_________________。
2NH3(g) △H=a kJ/mol。试根据表中所列键能数据估算a的数值:_________________。

(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知:
C(s,石墨)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1 ①
2H2(g)+O2(g)== 2H2O(I) △H2=-571.6kJ·mol-1 ②
2C2H2(g)+5O2(g)== 4CO2(g)+2H2O(I) △H3 =-2599kJ·mol-1③
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:____________。
查看答案和解析>>
科目:高中化学 来源:2017届重庆八中高三上学期定时训练14化学试卷(解析版) 题型:填空题
蓄电池是一种可以反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应是:NiO2+Fe +2H2O=Fe(OH)2+Ni(OH)2
(1)金属镍在元素周期表中的位置是______________。
(2)此蓄电池放电时,该电池发生氧化反应的物质是________(城序号)。
A. NiO2 B.Fe C. Fe(OH)2 D.Ni(OH)2
(3)此蓄留电池充电时,阳极的电极反应式是____________。
(4)用该蓄电池电解含有0.2molNaCl的混合溶液100mL,假如电路中转移了0.1mo电子,且电解池的电极均为惰性电极。阳极产生的气体在标准状况下的体积是________;将电解后的溶液加水稀释至1L,此时溶液的pH=________________。
(5)该电池电极材料对环境有危害。在对电池进行回收处理过程中遇到以下问题:己知:常温下Ksp[Fe(OH)3]=1.0×10-34,Ksp[Ni(OH)2]=1.0×10-15。某溶液中含有0.1mol/L的Ni2+和0.1mol/LFe3+,当逐滴加入NaOH溶液(忽略溶液体积改变),
①先沉淀的离子是________。
②要想使Fe3+沉淀完全,Ni2+不沉淀,溶液的pH需控制的范围是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com