
由FeSO4和Fe2(SO4)3组成的混合物中,含硫为a%,则所含铁的质量百分含量为
A.3a% B.(100-2a)% C.20% D.1-3a%
科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知水的电离平衡曲线如图所示,下列说法正确的是

A.水的离子积常数关系为:KW(B)>KW(A)>KW(C)>KW(D)
B.B点对应的温度下,pH=4的硫酸与pH=10的氢氧化钠溶液等体积混合,溶液的pH=7
C.向水中加入醋酸钠固体,可从C点到D点
D.升高温度可实现由C点到D点
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省赣州市北校区高二1月月考化学试卷(解析版) 题型:选择题
恒温恒容条件下,进行以下反应:H2(g)+ Br2(g) 2HBr(g),已知加入 l mol H2和 2mol Br2时,达到平衡后,生成 a molHBr。在相同条件下,起始时加人H2、Br2、HBr的物质的量分别为x、y、z(均不为零),如果仍保持平衡后各组分的物质的量分数不变,则以下推断不正确的是
2HBr(g),已知加入 l mol H2和 2mol Br2时,达到平衡后,生成 a molHBr。在相同条件下,起始时加人H2、Br2、HBr的物质的量分别为x、y、z(均不为零),如果仍保持平衡后各组分的物质的量分数不变,则以下推断不正确的是
A.达平衡时HBr物质的量一定仍为a mol
B.两平衡压强比为3:(x+y+z)
C.达平衡时HBr的物质的量为(x+y+z)a/3
D.x、y、z应满足的关系是 4x+z= 2y
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省赣州市北校区高二1月月考化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,可以再生,在使用过程中对环境无污染或污染很小。下列符合未来新能源标准的是
①天然气 ②风能 ③石油 ④太阳能 ⑤生物质能 ⑥煤 ⑦氢能
A.①④⑥⑦ B.②④⑤⑦ C.①②③⑥ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一12月月考化学试卷(解析版) 题型:选择题
将下列四种铁的化合物溶于稀盐酸,滴加硫氰化钾溶液没有颜色变化,再加入氯水即呈红色的是
A.FeS B.Fe2O3 C.FeCl3 D.Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一12月月考化学试卷(解析版) 题型:选择题
两份等质量的铝粉,一份投入足量的稀盐酸中,另一份投入足量的氢氧化钠溶液中,则生成氢气的质量比为
A.2:3 B.3:2 C.36.5:40 D.1:1
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二12月月考化学(选修)试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH- → CH3COOH+ C2H5O-
B.用银氨溶液检验乙醛的醛基:CH3CHO +2Ag(NH3)2+ + 2OH- 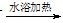 CH3COO- + NH4+ +3NH3 + 2Ag↓+ H2O
CH3COO- + NH4+ +3NH3 + 2Ag↓+ H2O
C.向苯酚钠溶液中通入少量的CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2CO32-
2C6H5OH + 2CO32-
D.甘氨酸与氢氧化钠溶液反应: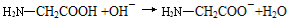
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一上学期期末化学试卷(解析版) 题型:填空题
(方程式每空2分,其余每空1分,共20分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O = 2NaOH + H2↑ ②2Na2O2 + 2H2O = 4NaOH + O2↑
③Na2O + H2O =2NaOH ④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+ O2↑ ⑥2F2 + 2H2O = 4HF + O2
2H2↑+ O2↑ ⑥2F2 + 2H2O = 4HF + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)
水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应? (填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是 。
(Ⅱ)写出下列反应的离子方程式:
①铜片与稀硝酸的反应:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入过量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②制漂白液的反应:
③雕刻花玻璃的反应:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com