
| A. | 任何气体单质在标准状况下体积约为22.4L,则含有2NA个原子 | |
| B. | 常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA | |
| C. | 常温常压下,11.2L甲烷(CH4)中含有的氢原子数为2NA | |
| D. | 标准状况下,0.3mol二氧化碳中含有氧原子数0.3NA |
分析 A、单质分为单原子分子、双原子分子和多原子分子;
B、氧气和臭氧均由氧原子构成;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、二氧化碳中含2个氧原子.
解答 解:A、单质分为单原子分子、双原子分子和多原子分子,故标况下22.4L气体单质的物质的量为1mol,但含有的原子个数不一定为2NA个,故A错误;
B、氧气和臭氧均由氧原子构成,故22g氧气和26g臭氧的混合物中含有的氧原子的物质的量为n=$\frac{22g+26g}{16g/mol}$=3mol,个数为3NA个,故B正确;
C、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L甲烷的物质的量小于0.5mol,含有氢原子小于2NA个,故C错误;
D、二氧化碳中含2个氧原子,故0.3mol二氧化碳中含0.6mol氧原子即0.6NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | Na2CO3 |
| B | Fe3O4 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
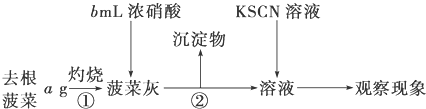
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
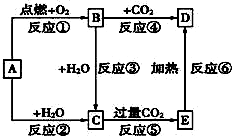 如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.已知A在空气中燃烧生成淡黄色固体(部分产物已略去).
如图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.已知A在空气中燃烧生成淡黄色固体(部分产物已略去). 查看答案和解析>>
科目:高中化学 来源: 题型:解答题
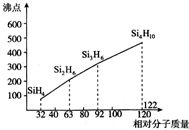 太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.
太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C6H6O6 | |
| B. | 乌头酸能使酸性高锰酸钾溶液褪色 | |
| C. | 含1 mol乌头酸的溶液最多可消耗3 mol NaOH | |
| D. | 乌头酸能发生水解反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①可用于分离C2H5OH和H2O的混合物 | |
| B. | 装置②可用于收集H2、Cl2等气体 | |
| C. | 装置③可用于有关NH3实验的尾气处理 | |
| D. | 装置④可用于洗涤BaSO4淀表面吸附的少量氯化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com