

| m(Sn) |
| m(ѳʷ) |
| 1.1424g |
| 1.226g |
| m(Sn) |
| m(ѳʷ) |
| 1.1424g |
| 1.226g |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| X |
| Y |
A”¢1£¼
| ||
B”¢3£¼
| ||
C”¢0.25£¼
| ||
D”¢0.25£¼
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ¢Ś
¢Ś ¢Ū
¢Ū ¢ÜHC”ŌCCH3 ¢ŻCH3CH2CH3 ¢ŽCH3CH=CHCH3£Ø””””£©
¢ÜHC”ŌCCH3 ¢ŻCH3CH2CH3 ¢ŽCH3CH=CHCH3£Ø””””£©| A”¢¢ŁŗĶ¢Ś | B”¢¢ŁŗĶ¢Ū |
| C”¢¢ŁŗĶ¢Ü | D”¢¢ŪŗĶ¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

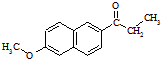 £©Ķā£¬×īæÉÄÜÉś³ÉµÄø±²śĪļ£ØÓėG»„ĪŖĶ¬·ÖŅģ¹¹Ģ壩µÄ½į¹¹¼ņŹ½ĪŖ
£©Ķā£¬×īæÉÄÜÉś³ÉµÄø±²śĪļ£ØÓėG»„ĪŖĶ¬·ÖŅģ¹¹Ģ壩µÄ½į¹¹¼ņŹ½ĪŖ £©µÄŃÜÉśĪļXŹĒCµÄĶ¬·ÖŅģ¹¹Ģ壬·Ö×ÓÖŠŗ¬ÓŠ2øöČ”“ś»ł£¬ĒŅČ”“ś»łŌŚĶ¬Ņ»øö±½»·ÉĻ£»XŌŚNaOHČÜŅŗÖŠĶźČ«Ė®½āŗó£¬ŗ¬ŻĮ»·µÄĖ®½ā²śĪļµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ5øö·å£®Š“³öXæÉÄܵĽį¹¹¼ņŹ½£ŗ
£©µÄŃÜÉśĪļXŹĒCµÄĶ¬·ÖŅģ¹¹Ģ壬·Ö×ÓÖŠŗ¬ÓŠ2øöČ”“ś»ł£¬ĒŅČ”“ś»łŌŚĶ¬Ņ»øö±½»·ÉĻ£»XŌŚNaOHČÜŅŗÖŠĶźČ«Ė®½āŗó£¬ŗ¬ŻĮ»·µÄĖ®½ā²śĪļµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ5øö·å£®Š“³öXæÉÄܵĽį¹¹¼ņŹ½£ŗ| SOCl2 |
 µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®| HBr |
| NaOH |
| ”÷ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ×°ÖĆ£ØĘųĆÜŠŌĮ¼ŗĆ£¬ŹŌ¼ĮŅŃĢķ¼Ó£© | ²Ł×÷ | ĻÖĻó |
 |
“ņæŖ·ÖŅŗĀ©¶·»īČū£¬ÖšµĪ¼ÓČėÅØ°±Ė® | ¢”£®CÖŠĘųĢåŃÕÉ«±äĒ³ ¢¢£®ÉŌŗó£¬CÖŠ³öĻÖ°×ŃĢ²¢Öš½„Ōö¶ą |


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| A”¢Ńõ»Æ¼ĮÓė»¹Ō¼Į±ŲŠėÖ±½Ó½Ó“„£¬²ÅÄÜ·¢Éś·“Ó¦ |
| B”¢ŅŅ³ŲÖŠµē¼«·“Ó¦Ź½ĪŖNO3-+4H++e-ØTNO2”ü+2H2O |
| C”¢µ±Ķ°ōÖŹĮæ¼õÉŁ6.4gŹ±£¬¼×³ŲČÜŅŗÖŹĮæŌö¼Ó6.4g |
| D”¢µ±Ķ°ōÖŹĮæ¼õÉŁ6.4gŹ±£¬ĻņŅŅ³ŲĆÜ·ā¹ÜÖŠĶØČė±ź×¼×“æöĻĀ1.12L O2£¬½«Ź¹ĘųĢåČ«²æČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ±ąŗÅ | ŹµŃéÄŚČŻ | ŹµŃéÄæµÄ |
| A | ŹŅĪĀĻĀ£¬ÓĆpHŹŌÖ½·Ö±š²ā¶ØÅضČĪŖ0.1mol?L-1 NaClOČÜŅŗŗĶ0.1mol?L-1 CH3COONaČÜŅŗµÄpH | ±Č½ĻHClOŗĶCH3COOHµÄĖįŠŌĒæČõ |
| B | Ļņŗ¬ÓŠ·ÓĢŖµÄNa2CO3ČÜŅŗÖŠ¼ÓČėÉŁĮæBaC12¹ĢĢ壬ČÜŅŗŗģÉ«±äĒ³ | Ö¤Ć÷Na2CO3ČÜŅŗÖŠ“ęŌŚĖ®½āĘ½ŗā |
| C | Ļņ10mL 0.2mol/L NaOHČÜŅŗÖŠµĪČė2µĪ0.1mol/L MgCl2ČÜŅŗ£¬²śÉś°×É«³Įµķŗó£¬ŌŁµĪ¼Ó2µĪ0.1mol/L FeCl3ČÜŅŗ£¬ÓÖÉś³ÉŗģŗÖÉ«³Įµķ | Ö¤Ć÷ŌŚĻąĶ¬ĪĀ¶ČĻĀµÄKsp£ŗ Mg£ØOH£©2£¾Fe£ØOH£©3 |
| D | ·Ö±š²ā¶ØŹŅĪĀĻĀµČĪļÖŹµÄĮæÅØ¶ČµÄNa2SO3ÓėNa2CO3ČÜŅŗµÄpH£¬ŗóÕß½Ļ“ó | Ö¤Ć÷·Ē½šŹōŠŌS£¾C |
| AӢA | BӢB | CӢC | DӢD |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com