
| A. | 在水中加入少量NaHCO3固体 | B. | 在水中滴入少量稀硫酸 | ||
| C. | 在水中加入少量氯化铝固体 | D. | 将水加热到100℃,测得pH=6 |
分析 能使水的电离平衡向右移动,说明加入的物质能和氢离子或氢氧根离子反应而促进水的电离;溶液呈酸性,说明加入的物质和氢氧根离子反应,导致溶液中氢氧根离子浓度小于氢离子浓度而使溶液呈酸性.
解答 解:A.碳酸氢钠中的碳酸氢根属于弱酸根离子,结合了水电离的氢离子,溶液显示碱性,故A错误;
B.硫酸电离出氢离子,抑制了水的电离,平衡向逆反应方向移动,故B错误;
C.氯化铝中的铝离子水解,促进了水的电离,平衡向正反应方向移动,溶液显示酸性,故C正确;
D.温度升高,水的电离平衡向正反应方向移动,溶液中的氢离子和氢氧根相等,溶液显示中性,故D错误.
故选C.
点评 本题考查了弱电解质的电离平衡,为高频考点,侧重考查学生的分析能力,明确酸或碱能抑制水的电离、含有弱酸根离子或弱碱离子的盐能促进水的电离是解本题关键,难度不大.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 过氧化钠投入到水中:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| B. | 氯化铵溶液与浓NaOH 溶液加热:NH4++OH-=NH3•H2O | |
| C. | 氯化铝溶液中滴入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+ | |
| D. | 实验室制取氯气:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2Cl-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 四种短周期元素X、Y、Z、W的部分信息如表:
四种短周期元素X、Y、Z、W的部分信息如表:| 元素 | 信息 |
| X | 原子半径最小 |
| Y | 单质在空气中含量最高 |
| Z | 其最外层电子数是电子层数的3倍 |
| W | 最高正价与最低负价的代数和为4 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤和水煤气均是二次能源 | |
| B. | 煤的干馏为化学变化,煤的液化和气化为物理变化 | |
| C. | 煤中含有苯、甲苯、二甲苯等有机物 | |
| D. | 由水煤气转化为甲醇或乙酸时,原子利用率均达到100% |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
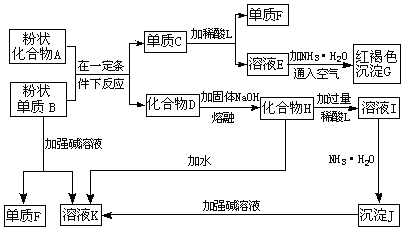
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
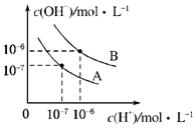 已知水在不同温度下的电离平衡曲线如图所示.(注:以下溶液混合时均不考虑体积的变化)
已知水在不同温度下的电离平衡曲线如图所示.(注:以下溶液混合时均不考虑体积的变化)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
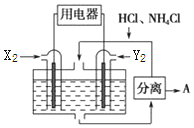
 如图是由常见元素组成的一些单质及其化合物之间的转化关系图.常温常压下,B、E、F、H、I均为气体,F无色无味,且能使澄清石灰水变浑蚀;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色.A是一种常见的氮肥,F也能由人直接分解可得到.C、G、K的焰色反应呈黄色.(反应中部分生成物己略去)
如图是由常见元素组成的一些单质及其化合物之间的转化关系图.常温常压下,B、E、F、H、I均为气体,F无色无味,且能使澄清石灰水变浑蚀;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色.A是一种常见的氮肥,F也能由人直接分解可得到.C、G、K的焰色反应呈黄色.(反应中部分生成物己略去)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
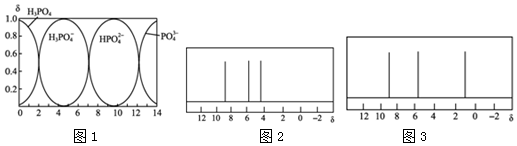
 ;分子M发生加聚反应产物的结构简式
;分子M发生加聚反应产物的结构简式 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com