
【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去).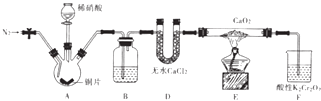
已知:2NO+CaO2═Ca(NO2)2;2NO2+CaO2═Ca(NO3)2
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2 , 原因是 .
(2)仪器D的名称是;B中盛放的试剂是 .
(3)装置F中,酸性K2Cr2O7溶液可将剩余的NO氧化成NO3﹣ , 溶液由橙色变为绿色(Cr3+),发生反应的离子方程式是 .
(4)已知Ca(NO2)2溶液需保持弱碱性,因为其遇酸会发生反应,产生NO气体.设计实验证明E中有亚硝酸钙生成 .
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2 , 反应原理为Ca(OH)2+NO+NO2=Ca(NO2)2+H2O.
①若n( NO):n(NO2)>1:1,则会导致:
②若n( NO):n( NO2)<1:1,则会导致 .
【答案】
(1)排除装置中氧气,防止其将生成的一氧化氮氧化生成二氧化氮
(2)U形干燥管,蒸馏水
(3)2NO+Cr2O72﹣+6H+=2Cr3++2NO3﹣+3H2O
(4)取少量E中反应后的固体于试管中,滴加少许硫酸,试管口有红棕色气体生成
(5)排放气体中NO含量升高,污染环境,产品Ca(NO2)2中Ca(NO3)2含量升高
【解析】解:(1)装置中含有空气,空气中氧气能氧化一氧化氮,所以通入氮气的目的是排除装置中氧气,防止其将生成的一氧化氮氧化生成二氧化氮;
(2)仪器D的名称是U形干燥管;硝酸易挥发,通过B中盛放的蒸馏水洗去硝酸,以防止过氧化钙反应生成氧气;
(3)反应中Cr2O72﹣被还原成Cr3+,NO氧化成NO3﹣,离子反应方程式为:2NO+Cr2O72﹣+6H+=2Cr3++NO3﹣+3H2O;
(4)Ca(NO2)2与酸会发生反应产生NO气体,NO气体遇氧气生成红棕色NO2气体,所以取少量E中反应后的固体于试管中,滴加少许硫酸,试管口有红棕色气体生成即可证明E中有亚硝酸钙生成;
(5)①若n(NO):n(NO2)>1:1,则一氧化氮过量,排放气体中NO含量升高,污染环境;
②若n(NO):n(NO2)<1:1,则二氧化氮过量,二氧化氮可与石灰乳反应生成Ca(NO3)2;
所以答案是:(1)排除装置中氧气,防止其将生成的一氧化氮氧化生成二氧化氮;(2)U形干燥管;蒸馏水;(3)2NO+Cr2O72﹣+6H+=2Cr3++NO3﹣+3H2O;(4)取少量E中反应后的固体于试管中,滴加少许硫酸,试管口有红棕色气体生成;(5)①排放气体中NO含量升高,污染环境;②产品Ca(NO2)2中Ca(NO3)2含量升高;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】由于Cl2对饮用水消毒,生成的有机氯化物对人体有害。世界环保联盟建议使用ClO2,它是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:KClO3+H2C2O4+H2SO4—— ClO2↑+K2SO4+CO2↑+H2O(未配平)。下列说法正确的是( )
A. KClO3在反应中是还原剂
B. 1 mol KClO3参加反应,在标准状况下能得到22.4 L气体
C. ClO2消毒的效率(以单位质量得到电子数表示)是Cl2的约5.3倍
D. 1 mol KClO3参加反应有1 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4的主要流程如下: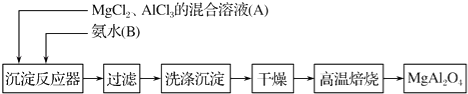
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式为 .
(2)判断流程中沉淀是否洗净所用的试剂是 .
(3)在25℃下,向浓度均为0.01mol/L的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式: .
【已知25℃时Ksp[Mg(OH)2]=1.8×10﹣11 , Ksp[Al(OH)3]=3×10﹣34】
(4)将Mg、Al组成的9.9g混合物投入一定量稀硝酸中,恰好完全反应,共收集到还原产物NO气体6.72L(标准状况),向反应后的溶液中加入4mol/L的Na0H溶液300mL时,则形成沉淀的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质发生化学反应时,下列选项在反应前后肯定不发生变化的是( )
①原子总数 ②分子总数 ③电子总数 ④物质的种类 ⑤物质的总质量
A.①②③B.①③⑤C.②③⑤D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“固体干冰→液体二氧化碳→气体二氧化碳→气体一氧化碳”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、范德华力
B.范德华力、范德华力、共价键
C.范德华力、共价键、共价键
D.共价键、共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中,Cl-、Br-、I-的物质的量分别为2mol、3mol、4mol;若通入一定量的氯气,使得溶液中Br-物质的量变为1mol,则通入氯气的物质的量为
A.1molB.2molC.3molD.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝诺酯主要用于类风湿性关节炎、风湿痛等.其合成路线如图所示: 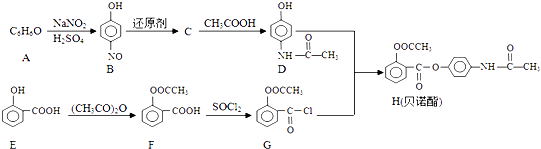
回答下列问题:
(1)A的结构简式为;E中含氧官能团的名称为 .
(2)D+G→H的反应类型为;C的结构简式为 .
(3)写出F与足量NaOH溶液反应的化学方程式: .
(4)写出符合下列条件的E的同分异构体结构简式 .
a.分子中含有苯环 b.能发生水解反应 c.核磁共振氢谱有4组峰
(5)请根据题中合成路线图有关信息,写出以甲苯和苯酚为原料制备 ![]() 的合成路线流程图(无机试剂可任选): .
的合成路线流程图(无机试剂可任选): .
合成路线流程图示例如下:CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3 .
CH3COOCH2CH3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应.请根据装置回答下列问题: 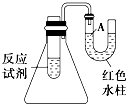
(1)将铝片加入小试管内,然后注入足量稀盐酸,有关反应的离子方程式是 , 试管中观察到的现象是 .
(2)U形导管中液面A(填“上升”或“下降”),原因是 , 说明此反应是(填“吸热”或“放热”)反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示.据图判断错误的是( ) 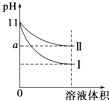
A.a的数值一定大于9
B.Ⅱ为氨水稀释时溶液的pH变化曲线
C.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
D.完全中和相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com