
(4分)在25mL 0.1 mol·L-1的NaOH溶液中逐滴加入0.2 mol·L-1的CH3COOH溶液,溶液pH变化曲线如图所示。
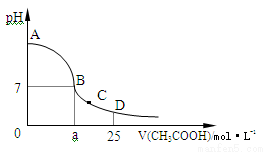
(1)B点溶液呈中性,有人据此认为,在B点时NaOH溶液与CH3COOH溶液恰好完全反应,这种看法是否正确? (填“是”或“否”),如果不正确,则二者恰好完全反应的点是在 (填“AB”、“BC”或“CD”)区间内。
(2)在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+)(填“>”、“<”或“=”)。
(3)在C点,溶液中离子浓度由大到小的顺序为: 。
(1)否 AB (2)= (3) c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
【解析】
试题分析:(1)NaOH溶液与CH3COOH溶液恰好完全反应,恰好生成CH3COONa,CH3COO—水解,此时溶液呈碱性,所以二者恰好完全反应的点在AB 区间内;(2)在D点时,25mL 0.1 mol·L-1的NaOH溶液含氢氧化钠0.0025 mol; 25mL 0.2 mol·L-1的CH3COOH溶液含CH3COOH0.005 mol;根据物料守恒,c(CH3COO-)+c(CH3COOH)=2c(Na+);(3)C点溶液中含有Na+、CH3COO-、H+、OH-,根据电荷守恒,c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-),C点溶液呈酸性,c(H+)> c(OH-),故c(Na+)<c(CH3COO-),所以离子浓度由大到小的顺序为:c(CH3COO-)> c(Na+)> c(H+)> c(OH-)。
考点:本题考查弱电解质电离和盐的水解。


科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:选择题
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为: a HClO3 = bO2↑+ c Cl2↑+ d HClO4 + e H2O。下列有关说法不正确的是
A.由反应可确定:氧化性HClO3>O2
B.若氯酸分解所得混合气体lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O
C.由非金属性Cl>S,可推知酸性HClO3>H2SO4
D.若化学计量数a=8,b=3,则该反应转移电子数为20e-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省莆田市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列说法或有关化学用语表达正确的是
A.二氧化碳的结构式:O—C—O
B.Cl-的结构示意图:
C.乙醇的结构简式:CH3CH2OH
D.过氧化氢(D2O2)的相对分子质量为34
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省英文学校高一上学期12月月考化学试卷(解析版) 题型:选择题
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是
①它们所含的分子数目之比为1∶1 ②它们所含的O原子数目之比为1∶2 ③它们所含的原子数目之比为2∶3 ④它们所含的C原子数目之比为1∶1 ⑤它们所含的电子数目之比为7∶11
A.①和④ B.②和③ C.④和⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(选做题16分)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为:CrO42-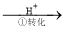 Cr2O72-
Cr2O72-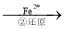 Cr3+
Cr3+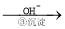 Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+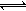 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,该溶液显 色。
(2)能说明第①步反应达平衡状态的是 。
A.Cr2O72-和CrO42-的浓度相同
B.2v (Cr2O72-)= v (CrO42-)
C.溶液的颜色不变
(3)第②步中,还原1molCr2O72-离子,需要 mol的FeSO4 7H2O。
7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在沉淀溶解平衡,请写出其沉淀溶解平衡方程式
常温下,Cr(OH)3的溶度积Ksp=[Cr3+]·[OH?]3=10?32,要使c(Cr3+)降至10?5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)用Fe做电极的原因是 。
⑹在阴极附近溶液pH升高的原因是(用电极反应解释) ,溶液中同时生成的沉淀还有 。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.常温下,将pH=3的醋酸溶液加水稀释到原体积的10倍后,溶液的pH=4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱 酸;若pH<7,则H2A是强酸
C.用0.2000 mol?L?1 NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1 mol?L?1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量AgCl固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1 mol/L氯化镁溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:选择题
已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1 mol·L-1 的 NaA和NaB混合溶液中,下列排序正确的是
A.[OH-]>[HA]>[HB]>[H+] B.[OH-]>[A-]>[B-]>[H+]
C.[OH-]>[B-]>[A-]>[H+] D.[OH-]>[HB]>[HA]>[H+]
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一上学期第三次考试化学试卷(解析版) 题型:选择题
为除去括号内的杂质,所选用的试剂或方法不正确的是
A.NaHCO3溶液(Na2CO3溶液) 通入过量的CO2
B.铁粉(铝粉) 加入适量的NaOH溶液过滤
C.Na2CO3溶液(Na2SO4溶液) 加入适量的Ba(OH)2溶液过滤
D.CO2 (CO) 将混合气体通过足量灼热的CuO
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次考试化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.③④⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.⑤⑥⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com