
下列关于有机化合物的叙述不正确的是
A.新制的氢氧化铜可以检验病人是否患有糖尿病
B.三氯甲烷可以做麻醉剂,它和四氯化碳都是重要的有机溶剂
C.根据金属钠与水、乙醇、乙酸反应剧烈程度的不同,可以说明分子中羟基上氢原子的活泼性不同
D.蛋白质、淀粉、纤维素水解的最终产物都是纯净物
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
某学生为了探究Zn与盐酸反应过程中的速率变化,在100mL稀盐酸中加入足量的Zn粉,用排水集气法收集反应放出的H2,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大 ,你认为原因是 。
(2)4~5 min时间段的反应速率最小,你认为原因是 。
(3)求2~3 min时间段内以盐酸的浓度变化来表示的反应速率(假设溶液体积保持不变)V(HCl)= 。
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O B.NaCl溶液 C.Na2CO3溶液 D.Cu粉 E.CuSO4粉末
你认为可行的是(填编号) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.3种元素的气态氢化物中Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z<Y<X
查看答案和解析>>
科目:高中化学 来源: 题型:
尽管氮元素在地壳中的丰度较低(主要以硝酸盐的形式存在),在所有元素中仅排31位,但是大气中有丰富的氮气,这为氨和硝酸的广泛应用提供了可能。
(1)氮气的电子式为 ,雷电作用能进行氮的固定,写出反应方程式 。
(2)食物蕴含的营养物质中,含氮的高分子化合物是 (填名称),其水解的最终产物为 。
(3)土壤中的NH4+在硝化细菌的催化作用下可转化为NO3﹣,写出其离子方程式: 。
(4)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。若沉淀质量为7.8g,则合金的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH。下列有关二甘醇的叙述正确的是
A.不能与金属钠发生反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D.符合通式Cn H2nO3
查看答案和解析>>
科目:高中化学 来源: 题型:
“瘦肉精”又称克伦特罗,其结构简式如右图。下列有关“瘦肉精”的说法不正确的
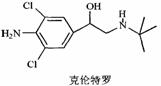 A.它的分子式为C12H18N2Cl2O
A.它的分子式为C12H18N2Cl2O
B.它含有氨基、氯原子等官能团
C.1mol克伦特罗最多能和3 molH2发生加成反应
D.一定条件下它能发生水解反应、酯化反应、消去反应、
氧化反应、加聚反应等
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸。
已知:
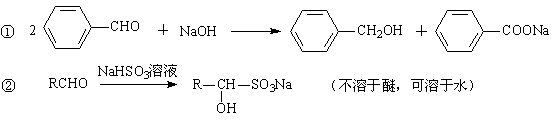
③苯甲酸易溶于乙醇,微溶于冷水,可溶于热水。
④乙醚沸点34.6℃,密度0.7138,易燃烧。当空气中含量为1.83~48.0%时易发生爆炸。
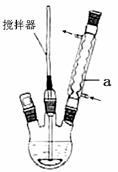 主要实验装置和步骤如下:
主要实验装置和步骤如下:
Ⅰ.向如图所示装置中加入8g氢氧化钠和30mL水,搅拌溶解,稍冷后
加入10 mL苯甲醛。在搅拌下反应40 min后,停止加热,从仪器a
上口加入冷水20 mL,冷却至室温。
Ⅱ.用乙醚萃取并分液。水层保留待用。醚层依次用少量饱和亚硫酸氢钠
溶液和蒸馏水洗涤后,分出醚层,倒入干燥的锥形瓶,加无水硫酸镁
干燥,注意锥形瓶上要加塞。将锥形瓶中溶液转入蒸馏装置,加热蒸出
乙醚;再升高温度,收集198℃~204℃的馏分得产品A。
Ⅲ.将步骤Ⅱ萃取后备用的水层慢慢地加入到盛有30 mL浓盐酸和30 mL水
的混合物中,同时用玻璃棒搅拌,析出白色固体。冷却,抽滤,得到粗
产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)写出玻璃仪器a的名称 ;其作用是 。
(2)步骤Ⅱ萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需 ,饱和亚硫酸氢钠溶液洗涤的目的是 ,
(3)产品A为 ,蒸馏除乙醚的过程中采用的加热方式为 。
(4)步骤Ⅱ用无水硫酸镁干燥时需要在锥形瓶上加塞,其原因是 。
(5)抽滤过程中需要洗涤产品晶体,下列液体最适合的是_______。
A.无水乙醇 B.饱和NaHCO3溶液 C.冷水 D.滤液
(6)停止抽滤的操作方法是 。提纯B的粗产品的实验操作名称为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
醇C5H11OH被氧化后可生成酮,该醇脱水时仅能得到一种烯烃,则这种醇是( )
A.C(CH3)3CH2OH B.CH(CH3)2CHOHCH3
C.CH3CH2CHOHCH3 D.CH3CH2CHOHCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com