
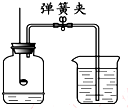
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )| A. | 实验时红磷一定过量 | |
| B. | 点燃红磷前先用弹簧夹夹紧乳胶管 | |
| C. | 红磷熄灭后立刻打开弹簧夹 | |
| D. | 最终进入瓶中水的体积约为氧气的体积 |
分析 要使实验准确,红磷的量要充足,不能使容器中气体逸出,红磷和氧气反应生成固体五氧化二磷,导致容器中压强减小,水进入容器中,进入水的体积就是氧气体积,据此分析解答.
解答 解:A.实验时红磷一定要过量,只有如此空气中氧气才能完全被消耗,误差才能较小,故A正确;
B.点燃红磷前先用弹簧夹夹紧乳胶管,防止气体逸出而导致测量不准确,故B正确;
C.红磷燃烧过程中产生热量导致压强增大,如果红磷熄灭后立刻打开弹簧夹会导致部分气体逸出而测量不准确,应该等冷却后再打开止水夹,故C错误;
D.红磷和氧气反应生成固体五氧化二磷,导致容器中压强减小,水进入容器中,进入水的体积就是氧气体积,故D正确;
故选C.
点评 本题考查空气中氧气含量测定,属于基础题,明确实验原理是解本题关键,注意操作步骤,会从实验的操作性及评价性进行分析判断,易错选项是C.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:解答题
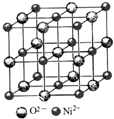 高氯酸三碳酰肼合镍{[Ni(CHZ)3](ClO4)2 }是一种新型的起爆药.
高氯酸三碳酰肼合镍{[Ni(CHZ)3](ClO4)2 }是一种新型的起爆药.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 实验室用图所示装置电解氯化铜溶液,实验中观察到碳(I)电极质量增加,碳(II)电极有气体放出.下列说法正确的是( )
实验室用图所示装置电解氯化铜溶液,实验中观察到碳(I)电极质量增加,碳(II)电极有气体放出.下列说法正确的是( )| A. | a为电源正极 | B. | 电极Ⅱ上发生还原反应 | ||
| C. | 电子流向:a→Ⅰ→Ⅱ→b | D. | 该装置将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,SO2、Cl- K+、HCO3-可以大量共存 | |
| B. | 和FeCl3溶液反应的离子方程式:S2-+Fe3+═Fe2++S | |
| C. | 和少量盐酸反应的离子方程式:S2-+H+═HS- | |
| D. | 1L0.1mol•L-1该溶液和足量硫酸铜溶液反应生成16.0克Cu2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃放烟花爆竹 | B. | 大力发展火力发电 | ||
| C. | 露天焚烧垃圾 | D. | 提高电动汽车的比例 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
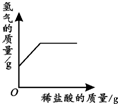
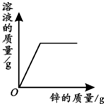
| A | B | C | D |
| 向一定量铁粉中滴加稀盐酸 | 向一定量硫酸铜溶液中不断加入锌粉 | 加热一定量高锰酸钾固体 | 向一定量氢氧化钠 溶液中滴加稀盐酸 |
 |  |  | 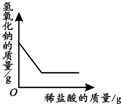 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡, 直至完全溶解. | 无气泡产生 | 猜想Ⅰ不成立 |
| ②取少量①中的溶液于试管中, 滴加CaCl2溶液. | 产生白色沉淀 | 证明有Na2CO3存在 |
| ③ 取少量①中的溶液于试管中,加入过量CaCl2溶液使沉淀完全,静置后,向上层清液中滴加酚酞试液. | 酚酞试液变红 | 证明有NaOH存在 |
| 综合以上实验现象,说明猜想Ⅱ是成立的. | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L<a<22.4L | |
| B. | 若a=16.8L,V(N2O4)=5.6L | |
| C. | 若a=16.8L,n(NaNO2):n(NaNO3)=4:1 | |
| D. | 若混合气体与NaOH溶液反应只生成一种盐,则n(NO)=0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W在元素周期表中位于笫三周期笫IVA族 | |
| B. | X的最简单气态氢化物的热稳定性比Y的强 | |
| C. | 由X、Y、Z三种元素组成的物质水溶液一定呈碱性 | |
| D. | 由Y、Z两种元素组成的离子化合物,其阳离子与阴离子个数比不一定为2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com