
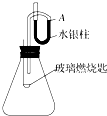
 ��֪����̼��CS2���ڳ����³�Һ̬��������������ȼ�����ɶ�����̼�Ͷ����������£�����ͼ��ʾ���װ�ã����������ѹǿ���ʱ��ˮ����Һ����A����ȡ����Ƥ�����ڲ���ȼ�ճ��м������̼���þƾ��Ƶ�ȼ����Ѹ��������ƿ�У���������Ƥ��������̼������ȼ�գ�A��ˮ����Һ���½���
��֪����̼��CS2���ڳ����³�Һ̬��������������ȼ�����ɶ�����̼�Ͷ����������£�����ͼ��ʾ���װ�ã����������ѹǿ���ʱ��ˮ����Һ����A����ȡ����Ƥ�����ڲ���ȼ�ճ��м������̼���þƾ��Ƶ�ȼ����Ѹ��������ƿ�У���������Ƥ��������̼������ȼ�գ�A��ˮ����Һ���½���
| ||
| ||
| ||
| ||
| ||
| ||


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������NaOH��Һ��Al+2OH-=AlO2-+H2�� |
| B������CO2ͨ��NaOH��Һ�У�CO2+2OH-=CO32-+H2O |
| C������ˮ��Ӧ��2Na+2H2O=2Na++2OH��+H2�� |
| D��ϡ�����еμ�����������Һ��H++OH-=H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
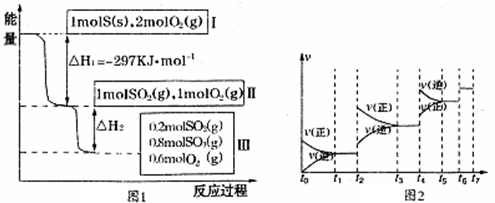
| n(SO3) |
| n(SO2) |
| t1-t2 | t3-t4 | t5-t6 | t6-t7 |
| K1 | K2 | K3 | K4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
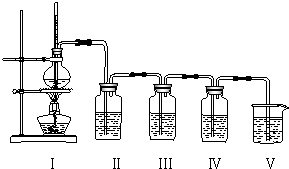
 ��ͼ��ͼ���в�������δ����������һ�ݻ�Ϊ300ml��ע��������һ500ml��������ƿ��������ƿ����0.384gͭƬ��������ƿ�м���18mL2.5mol��L-1��HNO3��Һ����������������ס����Ƥ����סƿ�ڣ��Իش�
��ͼ��ͼ���в�������δ����������һ�ݻ�Ϊ300ml��ע��������һ500ml��������ƿ��������ƿ����0.384gͭƬ��������ƿ�м���18mL2.5mol��L-1��HNO3��Һ����������������ס����Ƥ����סƿ�ڣ��Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����£���20mL0.2mol?L-1H2A��Һ�еμ�0.2mol?L-1NaOH��Һ���й��������ʵ����仯��ͼ������ͼʾ�жϣ�����˵����ȷ���ǣ�������
�����£���20mL0.2mol?L-1H2A��Һ�еμ�0.2mol?L-1NaOH��Һ���й��������ʵ����仯��ͼ������ͼʾ�жϣ�����˵����ȷ���ǣ�������| A��ͼ�Т����H2A�������HA-�������A2- |
| B����V[NaOH��aq��]=20mLʱ����Һ����ˮ�������c��OH-������10-7 mol?L-1 |
| C����V[NaOH��aq��]=40 mLʱ����Һ������Ũ�ȴ�С��ϵ��c��Na+����c��HA-����c��H+����c��A2-����c��OH-�� |
| D����NaHA��Һ����ˮ�Ĺ����У�pH��������Ҳ���ܼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����£���100 mL 0.1mol?L-1ijNaOH��Һ��ͨ��һ����CO2������������Һ�еμ�ijŨ�ȵ�ϡ���ᣬ�μ�������������������������ͼ��ʾ�����������ɵ�CO2ȫ���ݳ�������
����£���100 mL 0.1mol?L-1ijNaOH��Һ��ͨ��һ����CO2������������Һ�еμ�ijŨ�ȵ�ϡ���ᣬ�μ�������������������������ͼ��ʾ�����������ɵ�CO2ȫ���ݳ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com